Super-potenciadores sintéticos permiten una inmunoterapia viral de precisión contra el glioblastoma
Una investigación preclínica publicada en la revista Nature en abril de 2026 ha demostrado un método para la erradicación completa del glioblastoma agresivo en modelos de ratón mediante el uso de super-potenciadores sintéticos (SSE, por sus siglas en inglés). Esta tecnología permite la entrega precisa de cargas útiles anticancerígenas, logrando la eliminación del tumor tras una sola dosis.
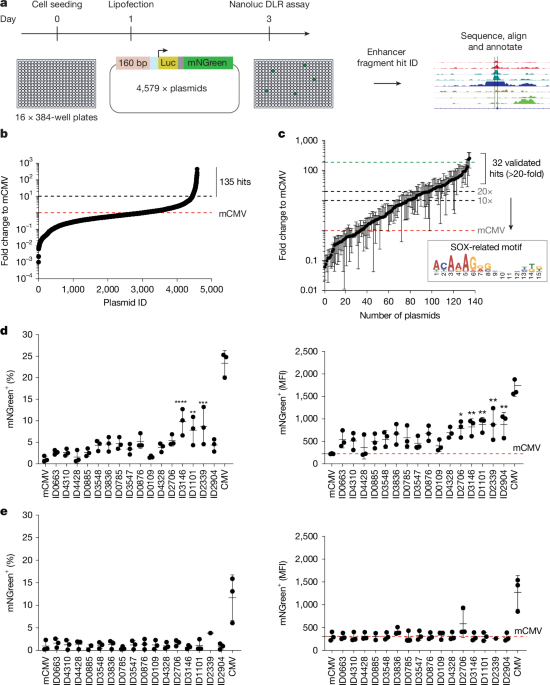
El enfoque se centra en las células madre del glioblastoma (GSC), dirigiéndose específicamente a las redes reguladoras transcripcionales impulsadas por SOX2 y SOX9. Para desarrollar los SSE, los investigadores ensamblaron fragmentos de potenciadores validados funcionalmente en matrices multipartitas, lo que resultó en una actividad robusta y una alta selectividad dentro de estos estados celulares específicos.
Superando las limitaciones de la terapia génica tradicional
Las terapias génicas convencionales suelen depender de promotores específicos de tipo celular para restringir la expresión de las cargas terapéuticas. Sin embargo, estos promotores frecuentemente presentan limitaciones en cuanto a su fuerza, tamaño y selectividad.
Los SSE están diseñados para superar estos obstáculos actuando como estaciones de acoplamiento para factores de transcripción que se expresan únicamente en células enfermas o cánceres agresivos. Análisis bioquímicos y datos de unión al genoma indican que estos elementos sintéticos integran factores de transcripción de estado de señalización y neurodesarrollo para activar la formación de grandes complejos multiméricos de factores de transcripción.
Resultados y validación
En el estudio, se utilizaron vectores de virus adeno-asociados para entregar una combinación de cargas útiles citotóxicas (HSV-TK y ganciclovir) e inmunomoduladoras (IL-12). Esta intervención única condujo a resultados curativos en el modelo de ratón con glioblastoma agresivo. Se observó que la IL-12 indujo una memoria inmunológica que previno la recurrencia del tumor.
La eficacia y selectividad tanto del virus adeno-asociado como de los SSE fueron validadas mediante el uso de muestras de corteza normal y tejido humano primario de glioblastoma. Los investigadores sugieren que este método, que aprovecha los programas transcripcionales centrales que definen el fenotipo de las GSC para permitir una activación inmunológica de precisión, podría tener aplicaciones más amplias en otros contextos donde se requiera un control preciso de la expresión de transgenes en estados celulares específicos.