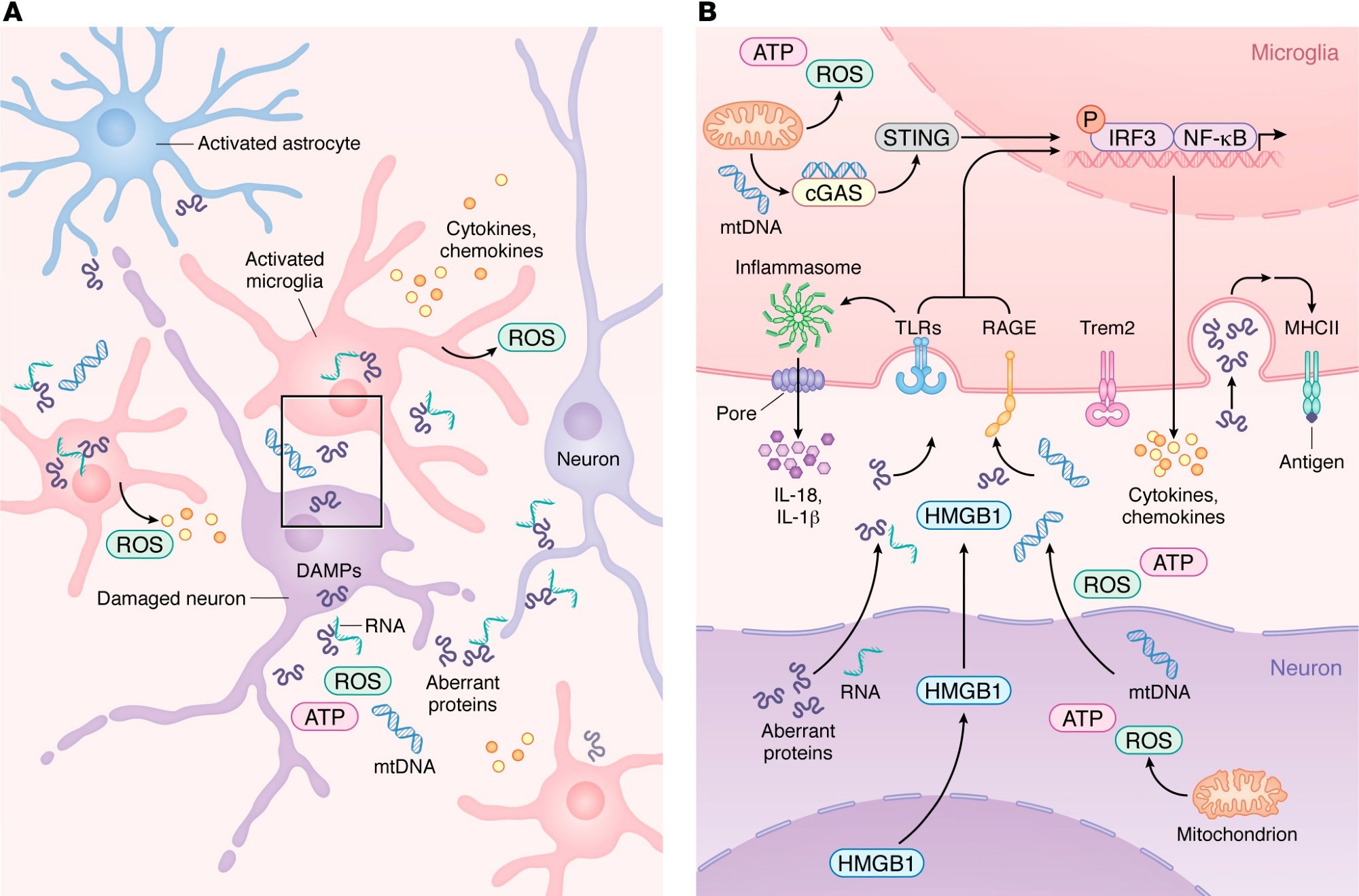
Un amplio estudio publicado recientemente revela cómo el sistema inmunológico del cerebro puede tanto combatir como contribuir al desarrollo de enfermedades neurodegenerativas como el Alzheimer, el Parkinson y trastornos relacionados. La investigación destaca que el momento, el tipo de célula involucrada y el contexto específico de la enfermedad son factores cruciales que podrían determinar el éxito de futuras terapias inmunomoduladoras.
central nervous system
Café y sueño: Estudio revela poca relación en adultos Estudio: El café no afecta significativamente el sueño ¿Interrumpe el café el sueño? Nuevo estudio lo cuestiona Café: Menos impacto en el sueño de lo que creías Sueño y café: ¿Realmente te quitan el descanso?
Un reciente estudio a gran escala publicado en la revista PLOS ONE sugiere que el consumo regular de café podría no alterar significativamente el sueño en adultos de mediana edad. Al analizar una amplia cohorte sueca, los investigadores encontraron poca o ninguna asociación entre la ingesta habitual de cafeína, la calidad del sueño y la somnolencia diurna.
El café y su reputación como perturbador del sueño, bajo nueva evaluación
El café es una de las bebidas más consumidas en el mundo, lo que convierte a la cafeína en su ingrediente psicoactivo más común. Se sabe que la cafeína promueve el estado de alerta al actuar sobre el sistema nervioso central (SNC) bloqueando los receptores de adenosina que regulan el equilibrio sueño-vigilia. Si bien la ingesta de cafeína a corto plazo se sabe que interrumpe el sueño, sus efectos a largo plazo siguen siendo poco claros.
Investigaciones genéticas emergentes demuestran además que las respuestas individuales a la cafeína varían. Los estudios de asociación del genoma completo (GWAS) vinculan variantes clave con las vías del metabolismo de la cafeína. En particular, los genes involucrados en el sistema del citocromo P450 (CYP450) y sus reguladores influyen en la eficiencia del procesamiento de la cafeína, lo que da forma a la tolerancia y los efectos fisiológicos. En este estudio, estos marcadores genéticos también se utilizaron para ayudar a validar la fiabilidad del consumo de café autoinformado.
Un amplio estudio de cohorte sueca examina la ingesta de café y la salud del sueño
En este estudio transversal, los investigadores examinaron la asociación entre el consumo habitual de café y la salud del sueño en 25.381 adultos de entre 50 y 64 años inscritos en el Estudio de Imagen Cardiopulmonar Sueco (SCAPIS).
El equipo evaluó la frecuencia de la ingesta de café en múltiples categorías de cuestionarios, que luego se agruparon en cuatro niveles (ninguno, bajo, moderado y alto) utilizando cuestionarios de frecuencia de alimentos (FFQ). Además, evaluaron los hábitos de sueño utilizando una versión modificada del Cuestionario Nórdico Básico del Sueño. También midieron la somnolencia diurna (SD) utilizando la Escala de Somnolencia de Epworth (ESS).
Los indicadores de la calidad del sueño incluyeron dificultad para conciliar el sueño, duración del sueño, despertares nocturnos, despertar temprano, reflujo después de acostarse, ronquidos fuertes y la calidad general del sueño. Los investigadores analizaron estos indicadores individualmente y como una puntuación compuesta del sueño.
Además, el equipo realizó GWAS para identificar variantes genéticas establecidas vinculadas a la ingesta de café y para validar el consumo de café autoinformado. Utilizaron modelos de regresión para estimar las razones de probabilidades ajustadas por factores de confusión identificados mediante el análisis de gráficos acíclicos dirigidos (DAG).
Además, los investigadores utilizaron modelos lineales generalizados cuasi-Poisson para evaluar las puntuaciones de sueño y somnolencia utilizando la ingesta de café como el predictor principal. Los análisis de sensibilidad probaron patrones de respuesta a la dosis utilizando cuatro enfoques de modelado. Estos incluyeron modelos categóricos, continuos y de spline no lineal para probar las asociaciones lineales y no lineales entre el consumo de café y los resultados del sueño.
El estudio revela vínculos mínimos entre la ingesta de café y la calidad del sueño
La cohorte incluyó ligeramente más mujeres (51%; n=12.990) que hombres. La mayoría de los participantes informaron que bebían café al menos una vez al día (88%; n=22.257). Los investigadores identificaron factores de confusión clave para la SD, incluido el edad, el sexo, el índice de masa corporal (IMC), la actividad física, el estrés, el tabaquismo, la ingesta de té, el uso de medicamentos para dormir y la duración del sueño nocturno. Los hombres fumadores con sobrepeso u obesos consumieron café con más frecuencia que sus pares.
GWAS identificó 66 polimorfismos de un solo nucleótido (SNP) asociados con la ingesta de café. Las variantes del receptor de hidrocarburos aromáticos (AHR), la proteína de unión a la calcineurina 1 (CABIN1) y la proteína que contiene el dominio sushi 2 (SUSD2) mostraron asociaciones negativas con una mayor ingesta. Por el contrario, las variantes cerca de CYP1A1/CYP1A2 mostraron asociaciones positivas, lo que respalda la fiabilidad de los datos de consumo de café autoinformados.
Los participantes generalmente informaron una buena calidad del sueño (puntuación media del sueño, 8,6) y solo el 16% experimentó somnolencia diurna excesiva. En general, la ingesta de café mostró asociaciones muy débiles con la calidad del sueño y la SD. Si bien varias asociaciones fueron estadísticamente significativas, su impacto práctico en el sueño fue muy pequeño.
Curiosamente, en comparación con los no bebedores, una baja ingesta de café se asoció con una peor calidad del sueño, mayor dificultad para conciliar el sueño y despertares nocturnos más frecuentes (razones de probabilidades de 1,16 a 1,17). Por el contrario, una alta ingesta se vinculó con una mejor calidad del sueño (razón de probabilidades, 0,83), menos dificultad para conciliar el sueño (razón de probabilidades, 0,86), menos despertares tempranos (razón de probabilidades, 0,78) y menos reflujo después de acostarse (razón de probabilidades, 0,82).
Aquellos con una mayor ingesta de café tuvieron ligeramente menos despertares nocturnos, aunque el hallazgo no fue estadísticamente significativo (razón de probabilidades, 0,92). No obstante, todos los niveles de ingesta se asociaron con ronquidos más fuertes (razón de probabilidades, 1,15-1,25). En general, los bebedores de café informaron ligeramente menos SD, pero una mayor ingesta no se tradujo constantemente en mayores beneficios.
Los hallazgos sugieren una posible adaptación biológica a largo plazo a la cafeína
Los hallazgos del estudio desafían la opinión común de que el consumo regular de café altera significativamente el sueño. Las asociaciones con la calidad del sueño y la somnolencia diurna fueron insignificantes, y los resultados estadísticamente significativos se tradujeron en diferencias mínimas en el mundo real. El IMC pareció modificar estos efectos, lo que indica que las personas con mayor adiposidad pueden ser más susceptibles a la alteración del sueño relacionada con la cafeína y podrían beneficiarse de una guía de ingesta personalizada. Los débiles vínculos también pueden reflejar una adaptación biológica a largo plazo, una hipótesis propuesta por los autores, ya que la exposición sostenida a la cafeína puede recalibrar la señalización de adenosina en el cerebro, particularmente en los adultos mayores.
Los análisis genéticos confirmaron marcadores conocidos cerca de AHR y CYP1A1/CYP1A2 e identificaron señales adicionales cerca de CABIN1 y SUSD2, lo que destaca posibles nuevas vías biológicas que vinculan la cafeína y el sueño. Sin embargo, los autores señalan que estos hallazgos son exploratorios y requieren una mayor investigación para determinar su relevancia biológica. Los futuros estudios deben utilizar medidas objetivas de la ingesta de cafeína y capturar información detallada sobre las fuentes y el momento del consumo. Los diseños longitudinales y comparativos por edad también ayudarán a aclarar los efectos a largo plazo y la susceptibilidad individual.
Un nuevo estudio publicado en la revista BIO Integration arroja luz sobre los mecanismos moleculares y celulares por los cuales un anticuerpo monoclonal agonista anti-TREM2 humano (hT2AB) podría mejorar la enfermedad de Alzheimer (EA). La EA, una enfermedad neurodegenerativa, es la principal causa de demencia en todo el mundo.
La investigación se centra en las microglías, células inmunitarias residentes en el sistema nervioso central (SNC), que desempeñan un papel crucial en la patología de la EA. Se ha observado que la acumulación de microglías alrededor de los depósitos de beta-amiloide (Aβ) es una característica distintiva de la enfermedad.
El receptor 2 expresado en células mieloides (TREM2) regula la función microglial, potenciando su respuesta al daño patológico de la EA, promoviendo la activación homeostática y modulando las vías protectoras. El hT2AB actúa como un ligando alternativo para TREM2 y ha demostrado potencial terapéutico en modelos de ratones con mutaciones en TREM2.
Este estudio combinó la secuenciación de ARN de células individuales (scRNA-seq) y la transcriptómica espacial para analizar la dinámica microglial en grupos tratados con hT2AB durante la progresión de la EA. Se identificaron subpoblaciones funcionales clave y biomarcadores centrales a través de análisis de pseudo-tiempo, análisis de comunicación celular y factores de transcripción (FT), con un enfoque en el proceso de diferenciación de las microglías hacia un fenotipo terapéutico.
Los análisis de scRNA-seq, transcriptómica espacial y deconvolución revelaron la complejidad de las microglías en la EA. El análisis pseudotemporal demostró las vías de diferenciación dinámica de las microglías durante la progresión de la enfermedad y después del tratamiento con hT2AB. Se identificaron siete subpoblaciones microgliales funcionalmente heterogéneas, destacando la subpoblación C2, que se expresó en mayor medida en el grupo tratado con hT2AB.
Las subpoblaciones relacionadas con Lineage1 (C7-C6-C4-C2-C1-C5) se alinearon con la transformación de las microglías hacia fenotipos protectores. El estudio también identificó biomarcadores centrales altamente expresados en la subpoblación C2, considerada un punto de inflexión clave en las dos trayectorias de diferenciación observadas. Además, el análisis de datos de transcriptómica espacial proporcionó evidencia directa de la distribución espacial de las subpoblaciones y vías clave.
Los resultados identificaron la subpoblación microglial C2 como el principal efector regulado por hT2AB en la patología de la EA. Se confirmó que hT2AB guía a las microglías hacia una diferenciación protectora, proporcionando evidencia a nivel celular del efecto terapéutico. Estos hallazgos profundizan la comprensión de la heterogeneidad de las microglías cerebrales en la EA y el mecanismo de acción de hT2AB, ofreciendo evidencia confiable para el desarrollo de nuevos biomarcadores y la optimización de terapias dirigidas a TREM2, con el potencial de mejorar los resultados clínicos en pacientes con EA.
Fuente:
Referencia del diario:
Sun, L., et. Al. (2026). Combined Analysis of Single Cell and Spatial Transcriptome Reveals Regulation of Anti-human TREM2 Agonist Monoclonal Antibody on the Functional Status of Microglia and Identification of Key Subsets and Biomarkers. BIO Integration. DOI: 10.1038/s43856-026-01432-w, https://www.scienceopen.com/hosted-document?doi=10.15212/bioi-2025-0179.
El consumo de nuez de betel, una práctica extendida pero a menudo subestimada, presenta riesgos significativos para la salud. Investigadores continúan buscando estrategias eficaces de prevención y tratamiento.
Una reciente revisión publicada en la revista Translational Psychiatry resume las características, mecanismos, consecuencias perjudiciales e intervenciones para la adicción a la nuez de betel. Esta sustancia psicoactiva es la cuarta más utilizada a nivel mundial, después del tabaco, el alcohol y las bebidas con cafeína. Aunque se ha utilizado en la medicina tradicional china y contiene diversos compuestos bioactivos, el consumo excesivo y prolongado de nuez de betel o productos quid (que a menudo incluyen tabaco u otros ingredientes) se ha asociado con un mayor riesgo de enfermedades, como el cáncer oral y las enfermedades cardiovasculares.
Se estima que alrededor de 600 millones de personas, principalmente en el sur de Asia, el Pacífico occidental y África oriental, consumen nuez de betel. India es el mayor consumidor, con casi una cuarta parte de los adultos que reconocen su uso. Los hombres son más propensos que las mujeres a combinar el consumo de nuez de betel con el tabaco y el alcohol, y la prevalencia en hombres es de tres a cinco veces mayor que en mujeres.
El consumo de nuez de betel suele comenzar a finales de la adolescencia y alcanza su punto máximo entre los 20 y los 40 años. Los factores socioeconómicos influyen en los patrones de uso, siendo más común entre personas que realizan trabajos físicamente exigentes o que requieren un estado de alerta sostenido, como taxistas, camioneros y trabajadores de la construcción, donde a menudo se utiliza como agente anti-fatiga. El estrés, un menor nivel educativo y unos ingresos familiares más bajos también se asocian con un mayor consumo.
El consumo prolongado de nuez de betel se ha relacionado fuertemente con la fibrosis submucosa oral, una condición con un alto riesgo de transformación en carcinoma de células escamosas oral. La carcinogenicidad es el riesgo para la salud más establecido, con fuertes asociaciones epidemiológicas entre el consumo de nuez de betel y la incidencia de cáncer oral. Los polifenoles de la nuez de betel y la arecolina, su principal compuesto bioactivo, pueden generar especies reactivas de oxígeno en condiciones alcalinas, lo que provoca daños en el ADN.
El consumo habitual también se ha asociado con un mayor riesgo cardiovascular, incluyendo inflamación, hipertensión, enfermedad cardíaca isquémica y aterosclerosis, aunque gran parte de la evidencia sigue siendo observacional. Estudios en ratones indican que los sistemas nervioso central y cardiovascular son los principales objetivos de la arecolina, que puede aumentar la frecuencia cardíaca, alterar la función endotelial y elevar la presión arterial a través de la activación del sistema nervioso simpático.
Estudios observacionales también han relacionado el consumo de nuez de betel con resistencia a la insulina, dislipidemia, obesidad y síndrome metabólico. Un estudio informó un riesgo 1,6 veces mayor de síndrome metabólico entre los consumidores en comparación con los no consumidores. También se ha asociado con proteinuria. Los efectos en el sistema nervioso central incluyen déficits neurocognitivos y, en algunos estudios, el uso prolongado y en dosis altas se ha asociado con síntomas psicóticos adversos, aunque los datos epidemiológicos a gran escala son limitados.
Las propiedades adictivas de la nuez de betel se atribuyen en gran medida a la arecolina, un agonista del receptor muscarínico de acetilcolina (mAChR) con afinidad por los subtipos de receptores M1 a M4. Esta activación colinérgica media la excitación y la vigilancia, produciendo efectos psicoestimulantes similares a los de la nicotina. Los alcaloides de la nuez de betel, incluyendo la arecaidina y la guvacolina, sufren transformaciones estructurales durante la masticación cuando se alcalinizan con cal, aumentando así la actividad del sistema nervioso central y la biodisponibilidad.
Estos alcaloides estimulan los mAChR, contribuyendo a los cambios de comportamiento. Las alteraciones en la dopamina extracelular dentro de los circuitos de recompensa cerebral se consideran centrales para el desarrollo de la adicción. Estudios in vivo sugieren que la arecolina afecta la transmisión de dopamina, mientras que estudios en animales muestran excitación de las neuronas dopaminérgicas, aumento de las tasas de disparo y ráfagas, y modulación de la señalización del glutamato y el ácido gamma-aminobutírico (GABA). Existe evidencia adicional que indica la participación de vías inmuno-inflamatorias e interacciones de señalización intestino-cerebro.
Actualmente no existe una farmacoterapia establecida para mitigar los síntomas de abstinencia. Dada la superposición neurobiológica con la dependencia de la nicotina, las terapias para dejar de fumar pueden ofrecer información valiosa. Algunas evidencias sugieren que el tratamiento con antidepresivos puede reducir la gravedad del consumo de nuez de betel, aunque las estrategias farmacológicas siguen siendo investigacionales, heterogéneas y carecen de protocolos estandarizados. Los inhibidores de la monoaminooxidasa y los inhibidores selectivos de la recaptación de serotonina se han propuesto como opciones de primera línea potenciales, pero la evidencia clínica sólida es limitada.
La terapia cognitivo-conductual (TCC) representa un enfoque de intervención fundamental. Los programas de TCC personalizados incorporan reestructuración cognitiva, entrenamiento en habilidades de afrontamiento y estrategias de prevención de recaídas. Un estudio informó tasas de cesación significativamente más altas entre los estudiantes después de tres meses de TCC en comparación con los controles. Otro ensayo que implementó una intervención conductual intensiva informó una reducción del 72 por ciento en el consumo, aunque la evidencia sigue siendo limitada en su alcance y requiere una validación más amplia. Estrategias emergentes como las tecnologías de neuromodulación, las intervenciones conductuales digitales y los enfoques de medicina de precisión están bajo investigación, pero se encuentran en etapas iniciales.
La adicción a la nuez de betel representa un complejo desafío de salud pública que requiere la colaboración multidisciplinaria en la prevención y el tratamiento. Se ha asociado con riesgos para la salud sistémica, consecuencias psicosociales e impactos económicos. El trabajo futuro debe centrarse en el establecimiento de redes de vigilancia, la estandarización de los métodos de recopilación de datos, la integración de modelos de intervención multidisciplinarios y la exploración de estrategias agrícolas alternativas para reducir la dependencia económica del cultivo de nuez de betel.
Referencia del artículo: Shao M, Zhuang L, Xie S, et al. (2026). Understanding betel nut addiction: a review of harmful consequences, underlying neurobiology, and emerging intervention strategies. Translational Psychiatry. DOI: 10.1038/s41398-026-03875-0. https://www.nature.com/articles/s41398-026-03875-0