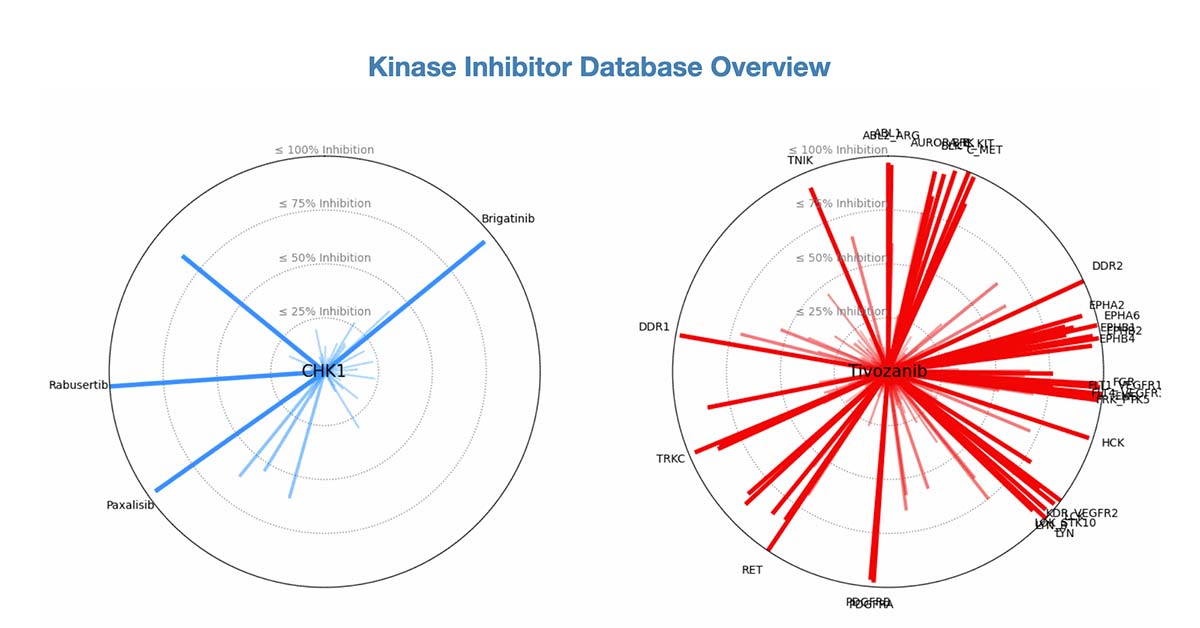
Un estudio reciente del Fred Hutch Cancer centre ha ampliado dramáticamente el rango terapéutico de los fármacos aprobados que actúan sobre quinasas, pasando de 89 a 235 inhibidores de quinasas aprobados por la FDA. Este hallazgo, publicado recientemente, tiene relevancia para múltiples tipos de cáncer.
La investigación, realizada mediante un perfilado bioquímico de 86 inhibidores de quinasas aprobados contra 758 quinasas (incluyendo 409 variantes salvajes y 349 oncológicas), reveló que el 94% de las mutaciones y el 97% de las fusiones identificadas en las muestras estudiadas pueden ser inhibidas por al menos un fármaco existente.
Entre los hallazgos validados experimentalmente se encuentran el uso de tepotinib para dirigirse a la vía IRAK1/4-colesterol en glioblastoma, brigatinib para atacar la vía MARK2/3-Hippo en cáncer pancreático y gilteritinib para superar la resistencia a fármacos y la metástasis impulsada por mutaciones en MET.
Para facilitar la exploración de estos datos, los investigadores han desarrollado KIRHub, una herramienta web que permite identificar inhibidores existentes de quinasas salvajes y mutadas con el objetivo de guiar la oncología de precisión.
El estudio subraya oportunidades significativas para el repositionamiento de inhibidores de quinasas ya aprobados, destacando especialmente la selectividad mutación-específica en quinasas tirosínicas como FGFR y MET, y señalando brechas actuales en el enfoque terapéutico.