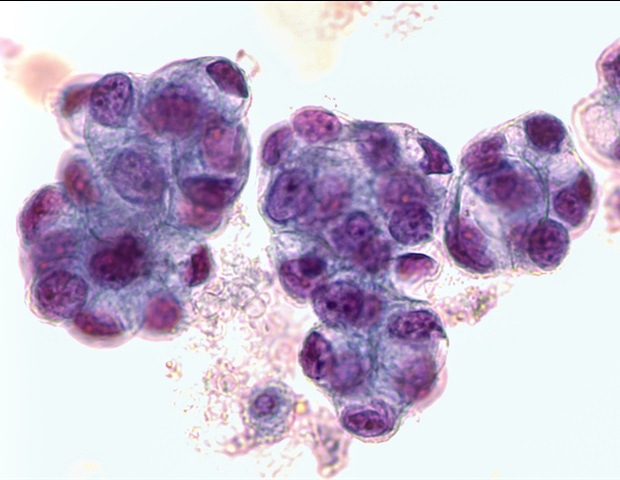
El adenocarcinoma cervical de tipo gástrico (GAS) es una de las variantes más agresivas de los adenocarcinomas cervicales no asociados al virus del papiloma humano (VPH), y representa un desafío significativo tanto para el diagnóstico como para el tratamiento médico.
Desafíos en el diagnóstico y tratamiento
Debido a que este tipo de cáncer puede originarse en la parte alta del canal cervical, dar resultados negativos en las pruebas de VPH y presentar una apariencia similar a la de las lesiones benignas, el GAS suele ser omitido durante el diagnóstico inicial. Clínicamente, se caracteriza por ser más invasivo, tener una mayor tendencia a la metástasis y estar vinculado a peores tasas de supervivencia en comparación con el adenocarcinoma endocervical de tipo habitual.
Además, los tratamientos estándar, como la quimioterapia y la radioterapia, suelen mostrar una eficacia limitada, y hasta hace poco la base biológica de esta resistencia terapéutica no estaba plenamente clara.
El papel de la clusterina en la progresión del tumor
Investigadores del Hospital de Obstetricia y Ginecología de la Universidad de Fudan, junto con laboratorios relacionados en Shanghái, han identificado un mecanismo clave en el desarrollo de esta enfermedad. En un estudio publicado el 6 de febrero de 2026 en la revista Precision Clinical Medicine, los científicos reportaron que el adenocarcinoma cervical de tipo gástrico desarrolla un programa de estrés distintivo asociado a la clusterina (CLU).
Esta proteína, la clusterina, impulsa la malignidad del tumor, facilita la evasión del sistema inmunológico y promueve la resistencia a la quimioterapia, creando un microambiente tumoral refractario al tratamiento.
Nuevas perspectivas terapéuticas
El estudio, que incluyó la revisión de 172 casos de adenocarcinoma cervical, reveló que la inhibición de la clusterina podría ser una vía efectiva para combatir el GAS. Específicamente, el uso de un agente anti-clusterina denominado OGX-011 mostró potencial para suprimir las características malignas del tumor y, fundamentalmente, sensibilizar la enfermedad al tratamiento con cisplatino.