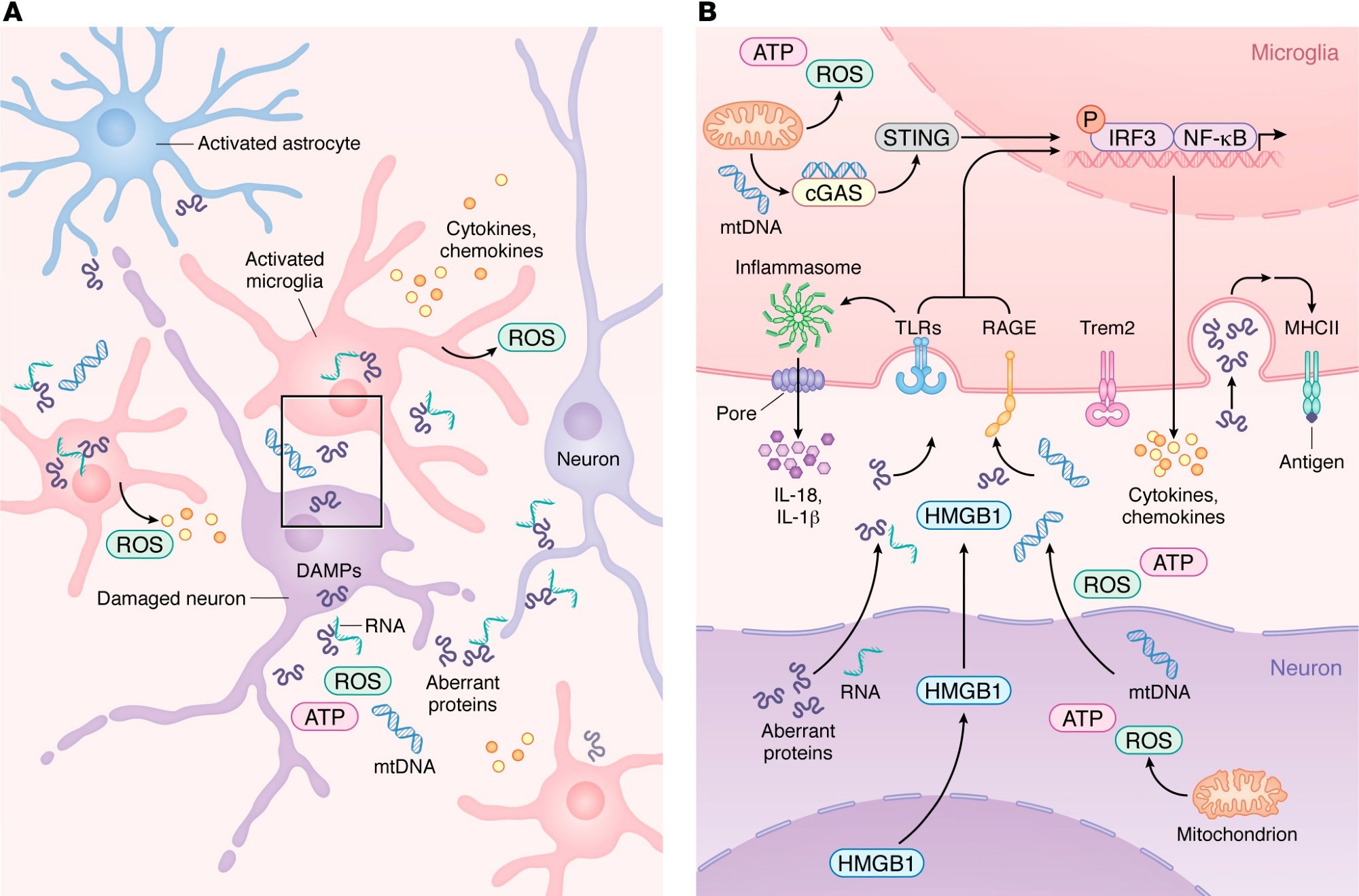
Un estudio reciente revela que las células inmunes del cerebro, conocidas como microglía, acumulan mutaciones genéticas asociadas al cáncer a medida que envejecen. Estas mutaciones, similares a las encontradas en cánceres de la sangre como leucemia y linfoma, no forman tumores, pero crean un entorno inflamatorio que daña las neuronas y podría contribuir al desarrollo del Alzheimer.
Los investigadores de Boston Children’s Hospital descubrieron que estas alteraciones genéticas somáticas —que ocurren después del nacimiento y no se heredan— están presentes en la microglía y podrían explicar parte de la neurodegeneración observada en la enfermedad de Alzheimer.
Este hallazgo sugiere que los medicamentos ya aprobados por la FDA para tratar ciertos cánceres de la sangre podrían ser reutilizados para frenar o detener el progreso del Alzheimer. Además, como estas mutaciones también se detectan en la sangre, abre la posibilidad de desarrollar una prueba genética sencilla para identificar a personas con alto riesgo mucho antes de que aparezcan los síntomas.
El estudio, publicado en la revista Cell, representa un avance importante en la comprensión de la mosaicism somático y su papel en enfermedades neurodegenerativas, ofreciendo nuevas vías para diagnóstico y tratamiento.