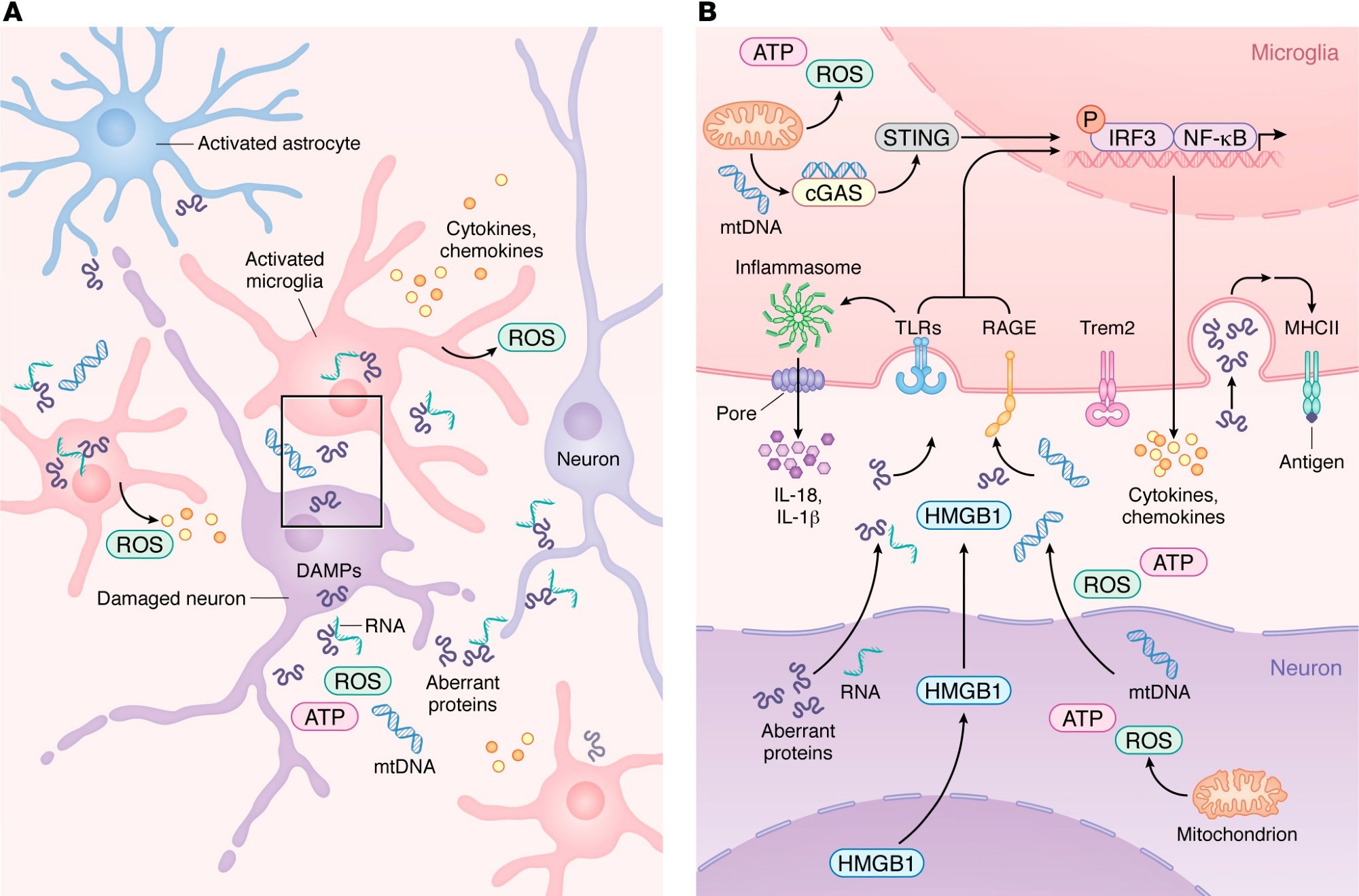
Un amplio estudio publicado recientemente revela cómo el sistema inmunológico del cerebro puede tanto combatir como contribuir al desarrollo de enfermedades neurodegenerativas como el Alzheimer, el Parkinson y trastornos relacionados. La investigación destaca que el momento, el tipo de célula involucrada y el contexto específico de la enfermedad son factores cruciales que podrían determinar el éxito de futuras terapias inmunomoduladoras.
Neurodegenerative Diseases
Alzheimer: Microglía, ¿aliada o enemiga en la propagación de la proteína Tau?
Investigadores del Glenn Biggs Institute for Alzheimer’s and Neurodegenerative Diseases en UT Health San Antonio han recibido una beca de $402,500 del Cure Alzheimer’s Fund para estudiar cómo las microglías, las células inmunitarias residentes del cerebro, podrían paradójicamente contribuir a la propagación de formas tóxicas de la proteína tau en la enfermedad de Alzheimer.
Sarah C. Hopp, PhD, profesora asociada de farmacología del Biggs Institute y del South Texas Alzheimer’s Disease Research Center, junto con su equipo, han sido fundamentales en el descubrimiento del comportamiento de las microglías. UT Health San Antonio es el centro de salud académico de The University of Texas at San Antonio.
A partir de este mes, el laboratorio de Hopp probará la hipótesis de que la captación de tau por las microglías es un mecanismo clave que impulsa su propagación por el cerebro, y que vías moleculares específicas determinan si este proceso protege o daña a las neuronas. El Cure Alzheimer’s Fund, también conocido como CureAlz, es una organización sin fines de lucro que financia investigaciones «con la mayor probabilidad de prevenir, ralentizar o revertir la enfermedad de Alzheimer».
Un artículo que describe el próximo estudio de Hopp, publicado en el sitio web de CureAlz y titulado «How Do Microglia Contribute to the Spread of Tau Pathology in Alzheimer’s Disease?» (¿Cómo contribuyen las microglías a la propagación de la patología de tau en la enfermedad de Alzheimer?), señala que, si bien los agregados de tau son una característica definitoria de la enfermedad de Alzheimer y están estrechamente relacionados con la pérdida de células cerebrales, los problemas de memoria y el deterioro cognitivo, todavía se desconoce mucho sobre cómo se propaga y qué papel juega el sistema inmunológico del cerebro en este proceso.
Existe evidencia, según el artículo, de que las formas tóxicas de tau, que se han «mal plegado» o vuelto disfuncionales, actúan como una «mala influencia».
«Cuando se encuentran con proteínas tau sanas cercanas, las hacen mal plegar también, desencadenando una reacción en cadena que se propaga de una región del cerebro a otra», según el artículo. «Las microglías… son de las primeras en encontrarse con estas ‘semillas’ tóxicas de tau. Normalmente, las microglías protegen el cerebro al eliminar desechos y ayudar a reparar el daño. Pero cada vez hay más evidencia que sugiere que las microglías también pueden contribuir a la propagación de tau al engullir tau mal plegado y liberarlo inadvertidamente, amplificando así sus efectos nocivos».
Las microglías estresadas pueden liberar toxinas
El artículo señala que el equipo de Hopp ya ha identificado la maquinaria celular que permite a las microglías internalizar tau y ha mapeado los puntos de control que determinan si las microglías destruyen con éxito el tau o lo liberan nuevamente al cerebro, encontrando que solo alrededor de una cuarta parte de las microglías captan tau mal plegado.
El equipo también ha descubierto que esta subpoblación expresa un conjunto único de genes relacionados con la endocitosis (el proceso por el cual las microglías engullen tau), el estrés en los centros de reciclaje de las células (lisosomas) y la migración.
Estos cambios sugieren que cuando las microglías ingieren demasiado tau, su capacidad para digerirlo adecuadamente se descompone, lo que las lleva a liberar señales inflamatorias y posiblemente a propagar el tau en lugar de eliminarlo, según el artículo.
Experimentos adicionales confirmaron este patrón: al principio, las microglías redujeron la acumulación de tau, pero con el tiempo, el estrés en sus lisosomas provocó que liberaran «semillas» de tau que podrían propagar aún más la patología.
El equipo también ha descubierto que el receptor LRP1 (para proteína relacionada con el receptor de lipoproteínas de baja densidad) es esencial para la captación de tau, ya que la eliminación de LRP1 redujo drásticamente la cantidad de tau internalizado por las microglías.
En conjunto, estos hallazgos sugieren que, si bien las microglías inicialmente ayudan a proteger el cerebro al eliminar el tau, el estrés prolongado o las vulnerabilidades genéticas pueden convertir este proceso protector en uno que empeora la enfermedad, según el artículo.
La nueva misión del equipo de Hopp
El equipo de Hopp perseguirá tres objetivos complementarios:
- Identificar qué hace que ciertas microglías sean más propensas a engullir tau que otras – Utilizando un mapeo avanzado de la expresión génica, microglías derivadas de células madre humanas y tejido cerebral post mortem de la enfermedad de Alzheimer, definirán la «huella digital» distinta de estas células que engullen tau. Esto ayudará a revelar qué características celulares o señales ambientales impulsan a las microglías hacia este papel especializado.
- Estudiar cómo las microglías pasan de ser limpiadoras de tau a propagadoras de tau – El equipo se centrará en dos procesos: la migración de las microglías y el sistema lisosomal o de reciclaje para determinar cuándo y cómo se rompen los roles protectores de las microglías. Comprender esta transición podría descubrir nuevos puntos de intervención para preservar la función saludable de las microglías.
- Probar si la captación de tau a través del receptor LRP1 es esencial para la progresión de la enfermedad – Utilizando ratones modificados genéticamente para que tengan microglías que carecen de LRP1, determinarán si bloquear esta vía ralentiza o previene la propagación de tau a través de las regiones cerebrales conectadas.
«En conjunto, estos estudios aclararán si las microglías actúan como barreras o aceleradores en la cascada de la enfermedad de Alzheimer», concluye el artículo. «Al identificar los interruptores moleculares que controlan este proceso, el trabajo de la Dra. Hopp podría abrir la puerta a nuevos tratamientos destinados a mantener las microglías en su modo protector, eliminando las proteínas tóxicas en lugar de ayudar a propagarlas».
El reciente discurso inaugural del premio Infosys 2025, a cargo del premio Nobel Randy Schekman, ofreció una perspectiva esperanzadora y a la vez preocupante sobre los avances en biología molecular y la edición del genoma, como en el caso de la anemia falciforme, así como sobre la creciente crisis de las enfermedades neurodegenerativas, con un enfoque particular en la enfermedad de Parkinson. Schekman describió el cerebro como “la gran frontera de la biología” debido a su inmensa complejidad y su papel fundamental en la definición de la naturaleza humana. Con miles de millones de células cerebrales y billones de terminales nerviosos, la comunicación selectiva entre estas células define nuestra identidad, influyendo en todos los procesos de pensamiento y emoción.
Una Enfermedad Sin Fronteras
Según Schekman, la enfermedad de Parkinson está aumentando en gravedad a nivel mundial, a un ritmo mayor que la enfermedad de Alzheimer. Estima que el 80% de los casos de Parkinson se deben a un proceso esporádico, probablemente causado por una toxina ambiental. Describe la propagación de la enfermedad como una “pandemia” que “no conoce fronteras”. Específicamente, predice que China representará más de la mitad de los nuevos casos diagnosticados en la próxima década, lo que atribuye no solo a una mejor capacidad de diagnóstico. Advirtió que, si bien China podría ser particularmente vulnerable al control de estas toxinas, otros países también se verán gravemente afectados. Aunque los estudios genéticos identifican alrededor de 20 mutaciones genéticas que causan formas familiares de la enfermedad, estas representan solo una pequeña fracción de los casos a nivel mundial.
La Vulnerabilidad de Nuestras Células Cerebrales
La teoría de la toxina ambiental resulta particularmente convincente debido a la extrema vulnerabilidad de las neuronas dopaminérgicas afectadas por la enfermedad de Parkinson. El profesor Schekman fue contundente al afirmar que estas células cerebrales están “al borde de la muerte”, requiriendo una enorme cantidad de energía para mantener su intrincada red de casi un millón de terminales nerviosos. “Cualquier pequeña agresión”, advirtió, “puede empujarlas al límite de la muerte”. Esto las hace excepcionalmente sensibles a las toxinas ambientales, presentes en entornos urbanos mal planificados. Cada neurona dopaminérgica posee una complejidad asombrosa, con cerca de un millón de terminales nerviosos que se conectan con otra estructura cerebral llamada estriado, responsable de las funciones ejecutivas y del movimiento, todas ellas comprometidas en pacientes con Parkinson.
La enfermedad se manifiesta mucho antes de que aparezcan los temblores. Los síntomas precursores, que pueden persistir durante años, incluyen una pérdida progresiva del olfato y un trastorno del comportamiento del sueño REM, donde los pacientes pierden el control de sus movimientos durante el sueño. Dentro de los cinco años, el 80% de estas personas progresa a la enfermedad de Parkinson. Estos son las señales de advertencia temprana del cuerpo de que algo en nuestro entorno está envenenando lentamente nuestras células cerebrales más vulnerables.
Una Tragedia Personal
La parte más conmovedora del discurso del profesor Schekman fue su relato honesto y desgarrador sobre la enfermedad de su difunta esposa, Nancy Walls, enfermera. Estuvieron casados durante 44 años y tuvieron dos hijos. Nancy enfermó de Parkinson a los 48 años. “Su neurólogo dijo que podría ser Parkinson”, recordó Schekman. “Ella preguntó, ¿cómo lo sabré?”. El médico le recetó una pastilla que básicamente reemplaza la dopamina. Schekman dijo que nunca olvidará la tarde en que ella lo llamó para informarle que, después de tomar la pastilla, todos los síntomas habían desaparecido en dos horas. “Esa era la buena y la mala noticia”, dijo en voz baja.
Recibió estimulación cerebral profunda a través de electrodos implantados bilateralmente en el cerebro medio para controlar las funciones motoras. Esto funcionó bien para aliviar los dolores y restaurar su movimiento. Desafortunadamente, al cabo de un año, comenzó a desarrollar síntomas de demencia. Como enfermera, sabía que una vez que se instalaba la demencia, solo empeoraría. En la ceremonia del Premio Nobel en 2013, Nancy sufrió de demencia de forma grave. Necesitaba ser sostenida y cuidada por sus familiares. Perdió la capacidad de comunicarse porque olvidaba lo que quería decir. Se volvió catatónica. Schekman le preguntó a sus neurólogos: «¿Qué puedo hacer para prepararme para la siguiente etapa?», pero sus respuestas fueron «siempre incorrectas». Necesitaba cuidados a tiempo completo, a menudo se caía debido a una presión arterial patológicamente baja y, algún tiempo después, murió en medio de la noche. “Nadie me dijo que esta es la frustración de las personas que cuidan a aquellos que padecen estos trastornos graves”. Su evidente dolor al recordar el momento provocó nudos en la garganta y lágrimas en los ojos de muchos en la audiencia.
La Búsqueda de una Cura
La enfermedad de Nancy influyó significativamente en la investigación y los esfuerzos filantrópicos posteriores de Schekman, y estableció becas y programas de investigación en su honor. Eugenia Brin, científica de la NASA, sufrió de Parkinson avanzado, y su hijo Sergey Brin, cofundador de Google, porta una mutación genética para la enfermedad. Sergey le pidió a Schekman que desarrollara un programa internacional de investigación básica que condujo a la creación de ‘Aligning Science Across Parkinson’s’ (ASAP). Durante los últimos siete años, la Fundación Sergey Brin Family ha comprometido más de mil millones de dólares para financiar a equipos de investigadores que colaboran por un propósito común en instituciones de todo el mundo. Michael J. Fox, diagnosticado con Parkinson a los 29 años, ha dedicado su vida a encontrar una cura y su fundación también apoya la investigación.
Las mejores mentes están trabajando para encontrar una solución, y es el trabajo colaborativo de los equipos lo que conducirá al éxito, cree Schekman. Hay 35 equipos en 163 laboratorios de todo el mundo, con investigadores en sus primeras etapas de carrera, muchos de ellos liderados por mujeres. Schekman concluyó con confianza que el programa ha identificado objetivos que la industria farmacéutica adoptará, lo que conducirá a avances y curas más eficaces en los próximos cinco años.
Pocos días después de escuchar la charla de Schekman, moderé una mesa redonda para ArtMantram sobre La Ciudad Consciente: Ecología, Bienestar y Futuros Urbanos. Los ponentes incluyeron al Dr. Issaac Mathai, Fundador de Soukya Holistic Health Centre, al Dr. Vivek Benegal, Profesor de Psiquiatría del NIMHANS; a Padma Shri Anita Reddy, activista social y fundadora de Dwaraka, y a Naresh Narasimhan, urbanista y arquitecto. Cada uno de ellos habló sobre los alarmantes efectos del urbanismo irreflexivo y su impacto en el bienestar físico y mental. La coincidencia de estos dos eventos, separados por apenas unos días, fue sorprendente. Con un premio Nobel advirtiendo que el 80% de los casos de Parkinson probablemente se deben a toxinas ambientales, y los principales expertos de la India en salud urbana describiendo los entornos tóxicos que estamos creando en nuestras ciudades, la conexión es innegable. La pregunta ya no es si podemos permitirnos ciudades ecológicamente racionales, sino si podemos permitirnos ignorar la necesidad de construirlas.
Sandhya Mendonca, autora, biógrafa, podcaster y editora de Raintree Media, ofrece una mirada femenina distintiva al mundo en esta columna.
Ejercicio reduce la edad cerebral: estudio revela beneficios a largo plazo
Un año de actividad aeróbica constante no solo mejoró la condición física, sino que también modificó la edad cerebral basada en imágenes de resonancia magnética (RM) en adultos de mediana edad, lo que sugiere que el ejercicio podría ayudar a preservar la salud cerebral mucho antes de la vejez.
Estudio: Efectos del estado físico y el ejercicio en la edad cerebral: Un ensayo clínico aleatorizado. Crédito de la imagen: Robert Kneschke/Shutterstock.com
Realizar ejercicio aeróbico de moderada a vigorosa durante 12 meses puede reducir un biomarcador de la edad cerebral, la diferencia de edad cerebral predicha (brain-PAD), en adultos jóvenes y de mediana edad, según un nuevo estudio publicado en la revista Journal of Sport and Health Science.
Los hábitos de ejercicio emergen como determinantes tempranos del envejecimiento cerebral
Los hábitos de vida, incluida la actividad física, desempeñan un papel vital en la modificación de los factores de riesgo de la mediana edad asociados con el deterioro morfológico y funcional del cerebro relacionado con la edad, la demencia y otras enfermedades neurodegenerativas. La actividad física regular en la mediana edad se ha relacionado con un menor riesgo de deterioro cognitivo y enfermedad de Alzheimer en la edad adulta tardía.
La evidencia existente indica que un impacto neural prolongado de la salud cardiometabólica y el estilo de vida comienza años antes de la manifestación clínica del deterioro cognitivo relacionado con la edad. A pesar del impacto significativo de los factores de riesgo cardiovasculares y del estilo de vida en la mediana edad en la salud cerebral, la mayoría de las intervenciones de ejercicio físico diseñadas para mejorar la aptitud cardiorrespiratoria (CRF) se han limitado a la edad adulta tardía.
Esta falta de intervenciones estratégicas destaca la necesidad de evaluar el impacto del ejercicio físico en la edad adulta temprana y media sobre los biomarcadores asociados con la salud cerebral relacionada con la edad y la edad cerebral estimada.
La evidencia mecanicista indica que el ejercicio mejora la salud cerebral al aumentar la CRF. Una CRF más alta se asocia con un mejor rendimiento cognitivo y un menor riesgo de demencia. La reducción inducida por el ejercicio de los factores de riesgo cardiometabólicos, como la presión arterial y el peso corporal, también se ha relacionado con una mejor salud cerebral.
Dada la importante asociación entre el ejercicio y la salud cerebral relacionada con la edad, investigadores del AdventHealth Research Institute y la Universidad de Pittsburgh, EE. UU., investigaron el efecto de una intervención de ejercicio aeróbico de 12 meses sobre la CRF y el brain-PAD, un marcador sustituto basado en neuroimagen del envejecimiento cerebral.
Un ensayo aleatorizado de un año prueba los efectos del ejercicio aeróbico
Este ensayo clínico aleatorizado de 12 meses incluyó a 130 participantes de entre 26 y 58 años que eran relativamente saludables pero físicamente inactivos. Fueron asignados aleatoriamente a un grupo de ejercicio aeróbico de intensidad moderada a vigorosa, intervención, o a un grupo de control de atención habitual, control.
Los participantes del grupo de intervención completaron dos sesiones supervisadas de 60 minutos por semana en un entorno de laboratorio, junto con ejercicio en el hogar, para alcanzar 150 minutos de ejercicio por semana.
El impacto del ejercicio en la CRF y la edad cerebral se evaluó al inicio y después de 12 meses. La edad cerebral se evaluó utilizando la diferencia de edad cerebral predicha, brain-PAD. Este biomarcador de neuroimagen cuantifica la diferencia entre la edad cronológica, la edad real, y la edad cerebral predicha derivada de la resonancia magnética estructural y los algoritmos de aprendizaje automático. El rendimiento cognitivo y los resultados de la demencia no fueron los puntos finales primarios de este ensayo.
También se analizó el impacto de posibles mediadores sobre el efecto del ejercicio en la edad cerebral. Estos mediadores fueron la composición corporal, la presión arterial y el factor neurotrófico derivado del cerebro (BDNF).
El ejercicio redujo la edad cerebral basada en la RM en casi un año
El estudio encontró una asociación significativa entre el aumento de la CRF y la reducción del brain-PAD al inicio. Este hallazgo indica que las personas con una mejor función cardíaca, pulmonar y vascular en la edad adulta temprana y media tienden a tener cerebros de apariencia más «joven» en la RM. Sin embargo, esta asociación transversal no mide directamente la tasa de envejecimiento cerebral ni predice las trayectorias de envejecimiento cerebral a largo plazo de cada individuo.
Después de 12 meses de intervención, los participantes del grupo de ejercicio mostraron una reducción media de aproximadamente 0,60 años en el brain-PAD, mientras que el grupo de control mostró un aumento no significativo de alrededor de 0,35 años. La diferencia entre los grupos correspondió a casi 1 año, 0,95 años, menos brain-PAD en el grupo de ejercicio en relación con los controles. No se observó tal mejora en la salud cerebral en el grupo de control después de 12 meses de atención estándar.
En cuanto a la CRF, el estudio encontró una mejora significativa en el consumo máximo de oxígeno, una medida de la aptitud cardiovascular y la resistencia aeróbica, a los 12 meses en los participantes del grupo de ejercicio. En contraste, los participantes del grupo de control mostraron una ligera reducción. No se observó un efecto significativo de la intervención de ejercicio sobre la composición corporal, la presión arterial o los niveles circulantes de factor neurotrófico derivado del cerebro. Sin embargo, el BDNF mostró un aumento marginal en el grupo de ejercicio en comparación con los controles.
El análisis de mediación, realizado para identificar posibles mediadores fisiológicos y biológicos de las asociaciones observadas, reveló que la mejora inducida por el ejercicio en la CRF no tiene una influencia significativa en la reducción inducida por el ejercicio del envejecimiento cerebral, según lo medido por el brain-PAD. De manera similar, no se observaron efectos de mediación de la composición corporal, la presión arterial y el factor neurotrófico derivado del cerebro sobre las asociaciones observadas.
El ejercicio en la edad adulta temprana y media se vincula a marcadores más saludables del envejecimiento cerebral
El estudio destaca la importancia de un programa de ejercicio aeróbico de intensidad moderada a vigorosa de 12 meses para mejorar la aptitud cardiorrespiratoria y reducir un marcador basado en neuroimagen del envejecimiento cerebral en adultos jóvenes y de mediana edad.
El estudio encuentra aproximadamente 1,83 años menos brain-PAD con cada desviación estándar de aumento en el consumo máximo de oxígeno, alrededor de 7 ml/kg/min. Estos hallazgos sugieren que las personas con una CRF más alta son menos vulnerables al envejecimiento cerebral de la mediana edad, según lo reflejado en las estimaciones de la edad cerebral basadas en la RM. La evidencia existente que vincula la CRF con el volumen de materia gris y la integridad de la materia blanca apoya aún más estos hallazgos.
En cuanto a los posibles mediadores de las asociaciones observadas, el estudio no encontró ningún efecto de la CRF en la reducción del envejecimiento cerebral inducida por el ejercicio. Una posible explicación es que los cambios inducidos por el ejercicio en la CRF, según lo medido por el consumo máximo de oxígeno, reflejan el componente modificable por el estilo de vida de la CRF. En contraste, los factores familiares, como el entorno compartido y los factores genéticos, contribuyen significativamente a la variación de la CRF cuando se mide de forma transversal.
Otra explicación sería que la influencia de la CRF puede ser más pronunciada en personas con un mayor riesgo cardiovascular. El estudio actual incluyó principalmente adultos jóvenes y de mediana edad relativamente saludables con bajo riesgo cardiovascular, lo que puede enmascarar cualquier mediación que solo surja en aquellos con patología vascular subclínica o manifiesta.
Los autores también señalan varias limitaciones, incluido el hecho de que solo alrededor del 62 por ciento de los participantes completaron la imagen cerebral post-intervención y que las interrupciones relacionadas con el COVID-19 afectaron las evaluaciones de seguimiento.
En general, los hallazgos del estudio sugieren que realizar actividad física moderada a vigorosa en la edad adulta temprana y media puede retrasar la progresión del envejecimiento cerebral según lo estimado por los biomarcadores de neuroimagen y podría reducir potencialmente el riesgo de demencia en la edad adulta tardía, pero se necesitan estudios a más largo plazo para determinar si estos cambios en el brain-PAD se traducen en beneficios cognitivos o clínicos sostenidos.
La exposición prolongada a la contaminación del aire podría aumentar el riesgo de desarrollar enfermedades neurodegenerativas graves, como la esclerosis lateral amiotrófica (ELA), y parece acelerar la progresión de estas enfermedades, según un estudio realizado por investigadores del Karolinska Institutet en Suecia. La investigación fue publicada en la revista JAMA Neurology.
“Podemos observar una clara asociación, a pesar de que los niveles de contaminación del aire en Suecia son más bajos que en muchos otros países. Esto subraya la importancia de mejorar la calidad del aire”,
Jing Wu, investigadora del Instituto de Medicina Ambiental, Karolinska Institutet
Las enfermedades de las motoneuronas (EMN) son afecciones neurológicas graves en las que las células nerviosas que controlan el movimiento voluntario se deterioran y dejan de funcionar, lo que provoca atrofia muscular y parálisis. La esclerosis lateral amiotrófica (ELA) es el tipo más común, representando entre el 85 y el 90 por ciento de los casos.
Factores ambientales como posibles contribuyentes
Si bien las causas de estas enfermedades son en gran medida desconocidas, se ha sospechado durante mucho tiempo que los factores ambientales juegan un papel importante. El nuevo estudio demuestra que la contaminación del aire podría ser uno de estos factores.
La investigación incluyó a 1.463 participantes en Suecia con diagnóstico reciente de EMN, quienes fueron comparados con 1.768 hermanos y más de 7.000 individuos de la población general. Los investigadores analizaron los niveles de partículas (PM2.5, PM2.5-10, PM10) y dióxido de nitrógeno en las direcciones de residencia de los participantes hasta diez años antes de su diagnóstico. Los valores medios anuales de estos contaminantes estaban ligeramente por encima de las directrices de la OMS, mientras que los valores máximos eran mucho más bajos que en países con alta contaminación atmosférica.
Un riesgo hasta un 30 por ciento mayor
La exposición a largo plazo a la contaminación del aire, incluso a niveles relativamente bajos típicos de Suecia, se asoció con un riesgo entre un 20 y un 30 por ciento mayor de desarrollar EMN. Además, las personas que habían vivido en áreas con mayores niveles de contaminación del aire experimentaron un deterioro más rápido de las funciones motoras y pulmonares después del diagnóstico. También presentaron un mayor riesgo de muerte y una mayor probabilidad de necesitar tratamiento con ventilación mecánica invasiva.
“Nuestros resultados sugieren que la contaminación del aire podría no solo contribuir al inicio de la enfermedad, sino también afectar la rapidez con la que progresa”, afirma Caroline Ingre, profesora adjunta del Departamento de Neurociencia Clínica del Karolinska Institutet.
Al centrar sus análisis en pacientes con ELA, los investigadores encontraron un patrón prácticamente idéntico al observado en todo el grupo de pacientes con EMN.
Inflamación y estrés oxidativo
Los investigadores enfatizan que el estudio no puede demostrar los mecanismos subyacentes a esta asociación, pero investigaciones previas indican que la contaminación del aire puede provocar inflamación y estrés oxidativo en el sistema nervioso. Dado que se trata de un estudio observacional, no se puede establecer una relación causal.
El estudio se basó en datos de registros suecos y fue financiado por diversas instituciones, incluido el Centro para el Control y la Prevención de Enfermedades de EE. UU., el Consejo de Investigación Sueco y el Karolinska Institutet.
Fuente:
Referencia del artículo:
Wu, J., et al. (2025). Long-Term Exposure to Air Pollution and Risk and Prognosis of Motor Neuron Disease. JAMA Neurology. doi: 10.1001/jamaneurol.2025.5379. https://jamanetwork.com/journals/jamaneurology/fullarticle/2843886
Alzheimer: Revelan estructura de la «capa difusa» de la proteína Tau
Uno de los sellos distintivos de la enfermedad de Alzheimer es la acumulación de proteínas llamadas Tau, que forman marañas fibrilares en el cerebro. Cuanto más severa es esta acumulación, más avanzada está la enfermedad.
La proteína Tau, también vinculada a numerosas otras enfermedades neurodegenerativas, se encuentra en un estado no estructurado en condiciones normales, pero en estados patológicos consiste en un núcleo rígido bien ordenado rodeado de segmentos flexibles. Estos segmentos desordenados forman una «capa difusa» que ayuda a determinar cómo interactúa Tau con otras moléculas.
Químicos del MIT han demostrado, por primera vez, que pueden utilizar la espectroscopía de resonancia magnética nuclear (RMN) para descifrar la estructura de esta capa difusa. Esperan que sus hallazgos contribuyan a los esfuerzos para desarrollar fármacos que interfieran con la acumulación de Tau en el cerebro.
Si queremos desagregar estas fibrillas de Tau con fármacos de moléculas pequeñas, entonces estos fármacos tendrán que penetrar esta capa difusa. Ese sería un futuro esfuerzo importante.
Mei Hong, profesora de química del MIT y autora principal del nuevo estudio
Jia Yi Zhang, estudiante de posgrado del MIT, es la autora principal del artículo, que aparece hoy en la Journal of the American Chemical Society. Aurelio Dregni, ex investigador postdoctoral del MIT, también es autor del estudio.
Analizando la capa difusa
En un cerebro sano, las proteínas Tau ayudan a estabilizar los microtúbulos, que proporcionan estructura a las células. Sin embargo, cuando las proteínas Tau se pliegan incorrectamente o se alteran de alguna otra manera, forman cúmulos que contribuyen a enfermedades neurodegenerativas como el Alzheimer y la demencia frontotemporal.
Determinar la estructura de las marañas de Tau ha sido difícil porque gran parte de la proteína –aproximadamente el 80 por ciento– se encuentra en la capa difusa, que tiende a ser muy desordenada.
Esta capa difusa rodea un núcleo interno rígido que está formado por hebras de proteínas plegadas conocidas como láminas beta. Hong y sus colegas ya habían analizado la estructura del núcleo en una fibrilla de Tau particular utilizando RMN, que puede revelar las estructuras de las moléculas midiendo las propiedades magnéticas de los núcleos atómicos dentro de las moléculas.
Hasta ahora, la mayoría de los investigadores habían pasado por alto la capa difusa de Tau y se habían centrado en el núcleo rígido de las fibrillas porque esos segmentos desordenados cambian sus estructuras con tanta frecuencia que las técnicas estándar de caracterización de la estructura, como la criomicroscopía electrónica y la cristalografía de rayos X, no pueden capturarlos.
Sin embargo, en el nuevo estudio, los investigadores desarrollaron técnicas de RMN que les permitieron estudiar toda la proteína Tau. En un experimento, pudieron magnetizar protones dentro de los aminoácidos más rígidos y luego medir cuánto tiempo tardaba la magnetización en transferirse a los aminoácidos móviles. Esto les permitió rastrear la magnetización a medida que viajaba desde las regiones rígidas hasta los segmentos flexibles, y viceversa.
Utilizando este enfoque, los investigadores pudieron estimar la proximidad entre los segmentos rígidos y móviles. Complementaron este experimento midiendo los diferentes grados de movimiento de los aminoácidos en la capa difusa.
«Hemos desarrollado ahora una tecnología basada en RMN para examinar la capa difusa de una fibrilla de Tau de longitud completa, lo que nos permite capturar tanto las regiones dinámicas como el núcleo rígido», afirma Hong.
Dinámica de las proteínas
Para esta fibrilla en particular, los investigadores demostraron que la estructura general de la proteína Tau, que contiene alrededor de 10 dominios diferentes, se asemeja un poco a un burrito, con varias capas de la capa difusa envueltas alrededor del núcleo rígido.
Basándose en sus mediciones de la dinámica de las proteínas, los investigadores encontraron que estos segmentos se dividían en tres categorías. El núcleo rígido de la fibrilla estaba rodeado de regiones proteicas con movilidad intermedia, mientras que los segmentos más dinámicos se encontraban en la capa exterior.
Los segmentos más dinámicos de la capa difusa son ricos en el aminoácido prolina. En la secuencia de proteínas, estas prolinas están cerca de los aminoácidos que forman el núcleo rígido y se pensaba que estaban parcialmente inmovilizados. En cambio, son muy móviles, lo que indica que estas regiones ricas en prolina con carga positiva son repelidas por las cargas positivas de los aminoácidos que forman el núcleo rígido.
Este modelo estructural proporciona información sobre cómo las proteínas Tau forman marañas en el cerebro, dice Hong. De forma similar a como los priones desencadenan el plegamiento incorrecto de proteínas sanas en el cerebro, se cree que las proteínas Tau mal plegadas se adhieren a las proteínas Tau normales y actúan como una plantilla que las induce a adoptar la estructura anormal.
En principio, estas proteínas Tau normales podrían agregarse a los extremos de los filamentos cortos existentes o apilarse en los lados. El hecho de que la capa difusa envuelva el núcleo rígido indica que las proteínas Tau normales es más probable que se agreguen a los extremos de los filamentos para generar fibrillas más largas.
Los investigadores planean ahora explorar si pueden estimular a las proteínas Tau normales para que se ensamblen en el tipo de fibrillas que se observan en la enfermedad de Alzheimer, utilizando proteínas Tau mal plegadas de pacientes con Alzheimer como plantilla.
La investigación fue financiada por los Institutos Nacionales de la Salud.
Una recientemente descubierta batalla molecular podría tener implicaciones importantes para comprender mejor el origen de múltiples enfermedades y trastornos – incluyendo cánceres, enfermedades neurodegenerativas y trastornos inmunitarios – así como para desarrollar posibles tratamientos, según investigadores de la Universidad Estatal de Pensilvania. El equipo realizó este hallazgo en un estudio de mensajeros celulares llamados ARNm, que transportan los planos del ADN necesarios para fabricar proteínas, los componentes básicos de la vida que mantienen el funcionamiento de las células. Después de entregar las instrucciones, estos mensajeros son eliminados por un complejo proteico llamado CCR4-NOT. Se pensaba que las proteínas en CCR4-NOT operaban en armonía, pero los investigadores señalan que no es así: una proteína desestabiliza el ARNm mientras que la otra lo estabiliza.
El equipo reveló esto en células de cáncer colorrectal humano utilizando una herramienta para desactivar temporalmente proteínas específicas. Al eliminar esencialmente una proteína, llamada CNOT1, CCR4-NOT ralentizó la eliminación del ARNm, pero al eliminar otra proteína de la célula, CNOT4, se aceleró el proceso de limpieza. Los detalles de la herramienta y sus análisis están disponibles en línea, a la espera de su publicación en un próximo número del Journal of Biological Chemistry.
«Tradicionalmente, se espera que las subunidades trabajen juntas hacia una función común, pero nuestros resultados muestran que CNOT4 tiene funciones únicas más allá de la degradación o catálisis del ARN», dijo Shardul Kulkarni, profesor asistente de bioquímica y biología molecular en la Universidad Estatal de Pensilvania, y primer autor del estudio. «Nuestro estudio demuestra que no todas las subunidades de un complejo de ‘degradación’ actúan de la misma manera: algunas pueden tener roles distintos e incluso opuestos. Comprender estas fuerzas opuestas nos brinda una imagen más clara de cómo las células mantienen un equilibrio en la expresión génica y podría indicar nuevas formas de intervenir cuando ese equilibrio se pierde».
Este equilibrio es fundamental para la regulación génica, que Kulkarni describió como un regulador de intensidad que aumenta o disminuye precisamente la luz para controlar cuándo, dónde y cuánto se utiliza cada gen, o con qué frecuencia se llevan a cabo las instrucciones para proteínas específicas. Kulkarni añadió:
«El estudio de la regulación génica es esencial para comprender la diferenciación celular, la progresión de una sola célula embrionaria a un organismo multicelular, y los mecanismos por los cuales los organismos se adaptan a los estímulos ambientales», dijo Kulkarni, explicando que, en condiciones de salud, los genes proporcionan los planos para cada componente biológico de un organismo, incluyendo el ARNm, pero eso no significa que el proceso sea precisamente el mismo todo el tiempo. «Nuestro hallazgo proporciona más información sobre cómo las moléculas involucradas en la regulación génica se equilibran o incluso se desafían mutuamente a medida que las células responden al estrés, la nutrición, la temperatura y otros cambios ambientales. Cuando ese sistema regulador falla, puede conducir a enfermedades como el cáncer, trastornos del desarrollo o problemas metabólicos».
Kulkarni trabaja en el laboratorio de Joseph C. Reese, profesor distinguido de bioquímica y biología molecular y autor corresponsal del estudio, en el Centro de Regulación Génica Eucariota de la Universidad Estatal de Pensilvania, donde se centran en CCR4-NOT, la máquina molecular que regula múltiples etapas del ciclo de vida del ARN. Esto se refiere a toda la existencia del ARN en las células: una proteína transcribe instrucciones del ADN al ARNm; el ARNm se procesa y empaqueta para que pueda moverse en la célula y proporcionar la información necesaria para fabricar una nueva proteína; y, finalmente, el ARN se descompone. Ese último paso, cuando el ARN se descompone y el mensaje se borra, está gobernado principalmente por CCR4-NOT.
CCR4-NOT fue descubierto por primera vez en levadura a principios de la década de 1990 y aparece en casi todas las células eucariotas, las células que componen todos los animales, plantas, hongos y muchos otros organismos. Si bien se sabe mucho sobre el complejo a partir de estudios con levadura, Kulkarni dijo que se comprende comparativamente menos el papel de CCR4-NOT en las células humanas. Para abordar esta brecha, el equipo desarrolló un sistema experimental para descubrir funciones previamente no caracterizadas de CCR4-NOT en células humanas.
Llamado sistema de degrón inducible por auxina (AID), la herramienta permite a los científicos «apagar» rápida y reversiblemente una proteína específica dentro de una célula, explicó Kulkarni. Funciona introduciendo una etiqueta a una proteína de interés que le indica a la célula que la destruya.
«Al poder destruir rápidamente las proteínas de interés, el sistema AID permite un control preciso de los niveles de proteína en las células humanas, lo que nos permite observar qué sucede cuando se elimina temporalmente una proteína específica», dijo Kulkarni.
Para probar el sistema AID, el equipo se centró en dos proteínas en CCR4-NOT en una línea celular comercial de cáncer colorrectal humano llamada DLD-1. La primera proteína, CNOT1, sirve como el andamiaje central de CCR4-NOT, mientras que la segunda, CNOT4, es una proteína menos comprendida involucrada en la regulación génica.
Con el sistema AID, los investigadores pudieron reducir completamente cualquiera de las dos proteínas en 60 minutos. Agotar CNOT1 alteró miles de transcripciones – las hebras simples de ARN que se transcriben a ARNm – y ralentizó la degradación del ARNm. Agotar CNOT4, por otro lado, no alteró mucho las transcripciones, pero promovió la degradación del ARNm.
«Comprender las complejidades de los efectos opuestos que CNOT1 y CNOT4 tienen sobre la estabilidad del ARNm tiene varias implicaciones», dijo Kulkarni, explicando que dicho conocimiento podría ayudar a identificar contextos de enfermedad en los que cualquiera de las subunidades esté desregulada, informar el desarrollo de biomarcadores basados en patrones característicos de degradación del ARNm y proporcionar información para estrategias terapéuticas que se dirijan a la estabilidad del ARNm y ajusten la regulación génica. «Con nuestro nuevo sistema, hemos abierto la puerta a aprender aún más».
Otros coautores afiliados al Centro de Regulación Génica Eucariota de la Universidad Estatal de Pensilvania son Courtney Smith y Oluwasegun T. Akinniyi, ambos estudiantes de posgrado en el programa de bioquímica, microbiología y biología molecular. Smith; Akinniyi; Belinda M. Giardine, programadora/analista; y Cheryl A. Keller, profesora de investigación, están afiliados al Departamento de Bioquímica y Biología Molecular de la Universidad Estatal de Pensilvania. Keller también es la directora del Centro de Genómica de la Universidad Estatal de Pensilvania en los Institutos Huck de las Ciencias de la Vida en la Universidad Estatal de Pensilvania. Alexei Arnaoutov, División de Biología Molecular y Celular en el Instituto Nacional de Salud Infantil y Desarrollo Humano de los Institutos Nacionales de Salud (NIH), también contribuyó a este trabajo.
Esta investigación fue posible gracias a varias instalaciones centrales administradas por los Institutos Huck de las Ciencias de la Vida en la Universidad Estatal de Pensilvania, incluyendo la Instalación Central de Proteómica y Espectrometría de Masas de Huck, la Instalación Central de Genómica, la Instalación Central de Citometría de Flujo y la Incubadora de Investigación Genómica.
Los NIH financiaron esta investigación.
Investigadores han desarrollado una nueva herramienta, FibrilPaint combinada con el test FibrilRuler, que permite a los científicos medir directamente la longitud de los fibrilos tóxicos de Tau en pequeñas muestras de fluidos, desde las primeras etapas de agregación hasta los fibrilos maduros e incluso a concentraciones muy bajas. Debido a que los fibrilos de Tau están estrechamente relacionados con el Alzheimer y otras demencias, pero han sido extremadamente difíciles de cuantificar en solución, esta “regla molecular” representa un avance significativo. Funciona en muestras complejas derivadas de pacientes y reconoce selectivamente los fibrilos amiloides de diversas enfermedades neurodegenerativas, lo que permite estudios mucho más precisos sobre cómo estos fibrilos crecen, se rompen y responden a posibles fármacos y, a largo plazo, podría sentar las bases para nuevas herramientas de diagnóstico o biomarcadores que rastreen la progresión de la enfermedad o la respuesta al tratamiento mediante la longitud de los fibrilos.
Un equipo de químicos y bioquímicos ha desarrollado una nueva y potente forma de medir el tamaño de los cúmulos de proteínas vinculados al Alzheimer y otras demencias relacionadas, en pequeñas muestras de fluidos y sin necesidad de una lámina de microscopio. La tecnología, denominada FibrilPaint y el test FibrilRuler, permite a los científicos determinar la longitud de los fibrilos de Tau directamente en solución, incluso a concentraciones muy bajas. El trabajo, liderado por el Prof. Assaf Friedler del Instituto de Química de la Universidad Hebrea y el Prof. Stefan G. D. Rüdiger de la Universidad de Utrecht, se publica en la revista Proceedings of the National Academy of Sciences (PNAS).
La enfermedad de Alzheimer y varios otros trastornos neurodegenerativos están relacionados con la acumulación de cúmulos anormales de la proteína Tau en el cerebro. Estos cúmulos, llamados fibrilos amiloides, crecen y cambian con el tiempo, y se cree que su desarrollo se correlaciona con la progresión de la enfermedad.
“La longitud de los fibrilos de Tau no es un simple detalle, sino un parámetro clave del proceso de la enfermedad”, afirmó el Prof. Friedler. “Hasta ahora, ha sido extremadamente difícil medir el tamaño de los fibrilos directamente en solución, especialmente a las minúsculas concentraciones que se encuentran en muestras biológicas reales.”
La mayoría de los métodos existentes requieren grandes cantidades de material, eliminan los fibrilos de su entorno natural o proporcionan solo información indirecta sobre el tamaño de los fibrilos. Esto ha limitado la capacidad de los científicos para estudiar cómo los fibrilos crecen, se rompen o responden a posibles fármacos y procesos biológicos.
En el corazón de este nuevo enfoque se encuentra FibrilPaint1, un péptido corto de 22 aminoácidos diseñado para actuar como un “marcador fluorescente” altamente selectivo para los fibrilos amiloides en fluidos.
FibrilPaint1 posee una combinación única de propiedades:
- Se une a los fibrilos de Tau con afinidad nanomolar, lo que significa que se adhiere firmemente incluso a concentraciones muy bajas.
- Reconoce precursores muy tempranos, hasta estructuras de solo cuatro capas de grosor, pero
- No se une a los monómeros de Tau, las moléculas de proteína individuales antes de que se agreguen.
- Lleva una etiqueta fluorescente, lo que permite a los investigadores ver y rastrear dónde y cómo se une.
- Reconoce una amplia gama de fibrilos de Tau, incluidos los derivados de pacientes con enfermedad de Alzheimer, degeneración corticobasal (DCB) y demencia frontotemporal (DFT).
- También se une a los fibrilos formados por otros amiloides relacionados con enfermedades, como el Amiloide-β, la α-sinucleína y la huntingtina, mientras
- Permanece altamente selectivo para el estado amiloide con una unión insignificante a agregados amorfos, suero sanguíneo o lisado celular.
“Queríamos una sonda que se comportara como una llave inteligente: que encontrara los fibrilos amiloides, incluidos los muy tempranos, e ignorara el resto del entorno biológico congestionado”, dijo el Prof. Rüdiger. “FibrilPaint1 hace exactamente eso.”
Para convertir esta sonda inteligente en una herramienta cuantitativa, el equipo combinó FibrilPaint1 con una tecnología de microfluidos llamada análisis de dispersión inducida por flujo (FIDA).
En el test FibrilRuler, FibrilPaint1 se une a los fibrilos amiloides en solución. Cuando la muestra fluye a través de una capilaridad microfluídica, la forma en que la señal fluorescente se extiende con el tiempo revela el tamaño efectivo del complejo fibrilo-FibrilPaint. A partir de esto, los investigadores pueden calcular la longitud del fibrilo con “resolución de capa”.
Utilizando esta configuración, el equipo pudo medir longitudes de fibrilos de Tau que oscilan entre solo 4 capas y 1.100 capas en solución, utilizando volúmenes de muestra submicrolítricos. Incluso a bajas concentraciones nanomolares, el método siguió siendo sensible y preciso.
“Es como tener una regla molecular dentro del propio fluido”, explicó el Prof. Friedler. “Ya no necesitamos inmovilizar los fibrilos en una superficie ni depender de grandes cantidades de material. Podemos seguir cómo los fibrilos crecen, se encogen o se fragmentan directamente en solución.”
Debido a que FibrilPaint1 reconoce los fibrilos de Tau derivados de pacientes con múltiples tauopatías y puede funcionar en mezclas biológicas complejas sin adherirse a otros componentes, el test FibrilRuler ofrece una plataforma atractiva tanto para la investigación básica como para futuras aplicaciones clínicas.
En el laboratorio, el método se puede utilizar para:
- Estudiar cómo los fibrilos se alargan o se rompen en diferentes condiciones.
- Probar cómo los fármacos o las vías biológicas modulan la longitud de los fibrilos.
- Comparar las propiedades de los fibrilos entre diferentes enfermedades o muestras de pacientes.
A largo plazo, los investigadores ven un potencial de uso diagnóstico.
“Si podemos medir directamente el tamaño de los fibrilos amiloides en material derivado de pacientes, por ejemplo, en líquido cefalorraquídeo u otras muestras accesibles, podríamos obtener un nuevo tipo de biomarcador para la demencia”, dijo el Prof. Rüdiger. “La longitud de los fibrilos es un parámetro informativo al que ha sido muy difícil acceder hasta ahora.”
“Nuestra visión es que el test FibrilRuler pueda adaptarse a una plataforma de diagnóstico para monitorizar la progresión de la enfermedad o la respuesta al tratamiento mediante el seguimiento del tamaño de los fibrilos a lo largo del tiempo. Si bien esto requerirá un mayor desarrollo y validación, este estudio es un primer paso importante”, añadió el Prof. Friedler.
Fuente:
Referencia del artículo: