Científicos han mapeado 239 virus de ARN que infectan a los humanos con el objetivo de rastrear y anticipar riesgos futuros de brotes. Este esfuerzo busca identificar patrones y características de estos virus para mejorar la preparación frente a posibles epidemias. El mapeo incluye información sobre su diversidad genética, mecanismos de infección y potencial para saltar entre especies, lo que podría ayudar a detectar amenazas emergentes con mayor antelación. Los investigadores destacan que comprender la evolución y el comportamiento de estos virus es clave para desarrollar estrategias efectivas de vigilancia y respuesta global.
RNA
Según un nuevo estudio publicado en la revista PLOS Biology, los ribosomas, conocidos como la maquinaria celular para fabricar proteínas, podrían actuar como «símbiontes egoístas» que han monopolizado los recursos celulares para impulsar la evolución desde el origen de la vida.
Los investigadores señalan que la formación de un solo ribosoma lleva aproximadamente siete minutos y que una célula bacteriana en rápido crecimiento puede contener entre 20.000 y 27.000 de estas estructuras. Más de la mitad de la energía celular se dedica a su creación y mantenimiento, y entre el 95 y el 98 por ciento del ARN celular corresponde a ARN ribosómico.
Debido a esta alta dependencia de los ribosomas, los virus no pueden producir los suyos propios y deben apropiarse de los de la célula huésped para replicarse. Por ello, los propios virus son considerados entidades dependientes de los ribosomas.
El sitio catalítico central del ribosoma es una «ribozima», una molécula de ARN capaz de realizar funciones catalíticas sin proteínas, lo que se interpreta como un remanente del hipotético «mundo del ARN», precedente a la aparición de las proteínas.
Un hallazgo reciente desafía el principio establecido de la síntesis de ADN, que ha dominado los libros de texto de biología durante décadas. Un equipo de investigadores de la Universidad de Stanford descubrió una enzima bacteriana capaz de sintetizar ADN utilizando una estructura proteica como molde, en lugar de depender de una cadena de ADN o ARN.
En la síntesis convencional de ADN, una polimerasa lee una cadena de ADN o ARN como molde y une bases nitrogenadas complementarias para formar una nueva hebra. Este mismo principio se aplica en la transcripción inversa, donde el ARN sirve como molde para producir ADN.
Sin embargo, al analizar los mecanismos de defensa de bacterias contra virus (fagos), el equipo identificó el sistema DRT3, que se desvía de esta regla establecida. DRT3 es un complejo formado por dos tipos de transcriptasas inversas y una molécula de ARN. Una de estas enzimas sintetiza ADN de cadena simple utilizando ARN como molde, siguiendo el proceso convencional.
La otra enzima, denominada Drt3b, funciona de manera distinta: utiliza aminoácidos presentes en su sitio activo como si fueran un molde de ARN para dirigir la síntesis de una hebra de ADN. En este caso, la estructura proteica en sí misma actúa como el plano para la producción de ADN.
Los investigadores señalaron que, dado que el sistema DRT3 se encuentra en diversas bacterias, este nuevo mecanismo de síntesis de ADN podría ser un proceso común más que una excepción rara. Aunque aún no se ha revelado exactamente cómo DRT3 inhibe a los bacteriófagos, su descubrimiento abre nuevas posibilidades en biotecnología, potencialmente comparable al impacto de sistemas como CRISPR, que también se originó en mecanismos de defensa bacteriana.
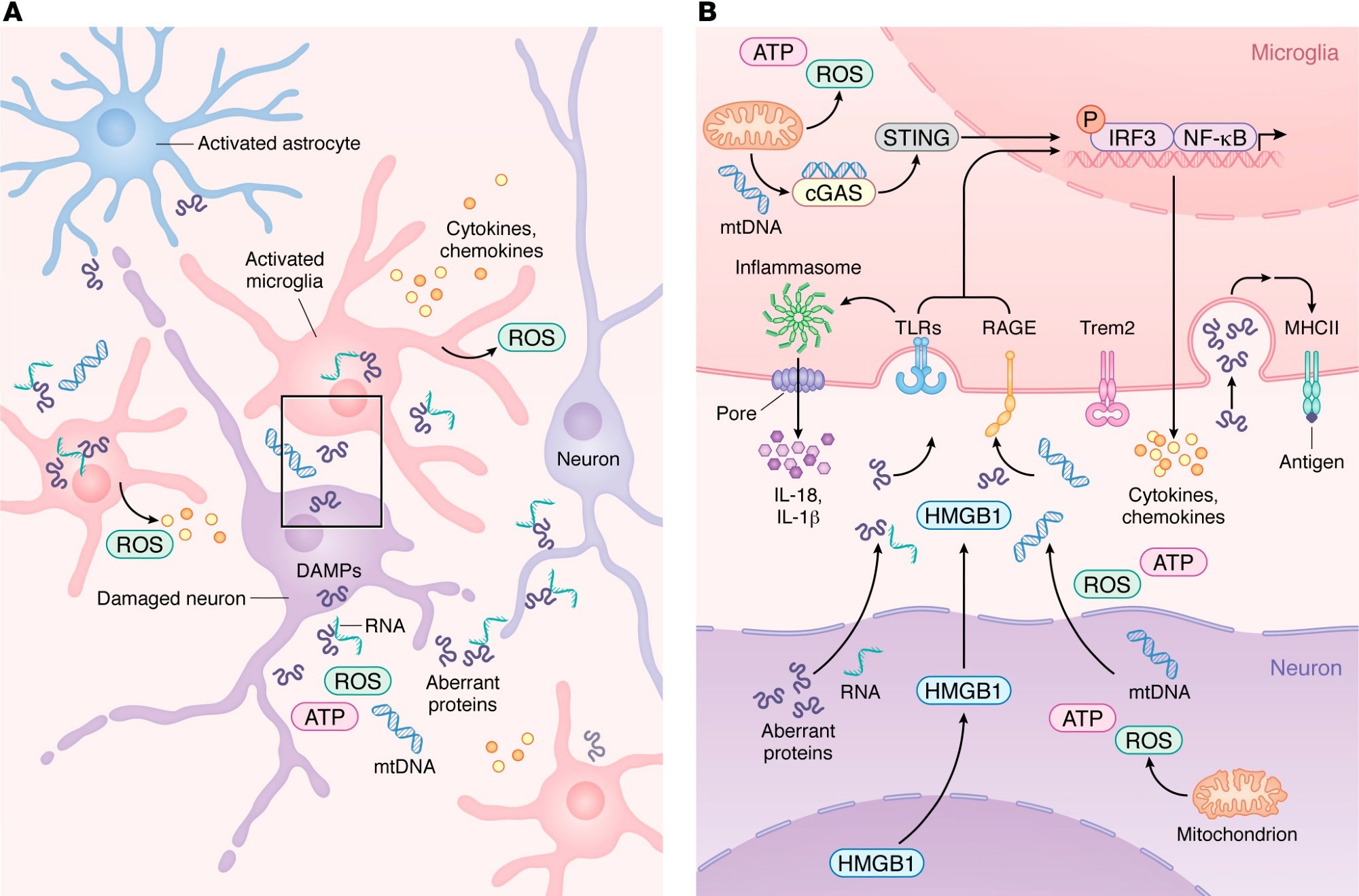
Un amplio estudio publicado recientemente revela cómo el sistema inmunológico del cerebro puede tanto combatir como contribuir al desarrollo de enfermedades neurodegenerativas como el Alzheimer, el Parkinson y trastornos relacionados. La investigación destaca que el momento, el tipo de célula involucrada y el contexto específico de la enfermedad son factores cruciales que podrían determinar el éxito de futuras terapias inmunomoduladoras.
El papel del complejo de nucleoproteína-ARN en la síntesis viral
El complejo de nucleoproteína-ARN en diversos virus cumple funciones críticas para la supervivencia del patógeno, ya que se encarga de proteger el ARN genómico y de brindar soporte a la síntesis de ARN viral. Debido a esto, comprender la estructura de este complejo es fundamental.
En el caso del virus de la enfermedad de Borna 1, los genomas de ARN son encapsidados por múltiples copias de la molécula de nucleoproteína viral (N), las cuales forman complejos N-ARN.
Por su parte, el virus sincitial respiratorio posee un complejo de nucleoproteína-ARN que forma una nucleocápside (NC) helicoidal zurda. Esta estructura, que comprende el genoma viral de ARN de sentido negativo, es esencial para que la ARN polimerasa dependiente de ARN del virus pueda llevar a cabo la síntesis de ARN.
Los ARN de vesículas extracelulares (EV-RNAs) representan una nueva esperanza para el diagnóstico y el tratamiento de la enfermedad inflamatoria intestinal (EII) crónica.
Estas moléculas presentan un potencial dual en el abordaje de la EII. Por un lado, pueden actuar como biomarcadores no invasivos, lo que facilitaría tanto el diagnóstico temprano como el monitoreo de la enfermedad.
Por otro lado, los EV-RNAs pueden funcionar como transportadores de ARN reguladores diseñados para combatir la inflamación, reparar la barrera epitelial y restablecer la homeostasis intestinal.
La infiltración de neutrófilos es una característica distintiva de la inflamación pulmonar durante las infecciones virales respiratorias, aunque el origen de estas células ha sido objeto de debate. Un estudio liderado por el equipo del profesor Xuetao Cao, de la Academia China de Ciencias Médicas, utilizando un modelo de hámster dorado infectado con SARS-CoV-2, ha revelado un eje dinámico de neutrófilos entre la vesícula biliar y el pulmón que opera durante la defensa antiviral. Los resultados de la investigación fueron publicados en línea en el Volumen 2 de la revista Immunity &. Inflammation el 11 de marzo de 2026.
El equipo integró el análisis de velocidad del ARN de una sola célula con la deconvolución transcriptómica espacial para rastrear la dinámica de los neutrófilos a lo largo del tiempo y en diferentes tejidos. Lo que surgió fue una clara imagen de la comunicación inter-orgánica: en el punto álgido de la respuesta antiviral, los neutrófilos originarios del bazo migran al pulmón, reponiendo las reservas locales en varias etapas de diferenciación y participando activamente en la defensa inmunitaria innata.
La investigación comenzó con un análisis detallado de la cinética de las células inmunitarias pulmonares. El perfilado de velocidad del ARN de una sola célula del tejido pulmonar al séptimo día post-infección reveló una trayectoria de diferenciación unidireccional dentro del compartimento de neutrófilos, desde un subconjunto proliferativo a través de etapas inmaduras y maduras hasta células completamente activadas. Es importante destacar que las fases proliferativa y de activación fueron temporal y transcripcionalmente distintas, lo que sugiere que la proliferación local por sí sola no podría explicar la magnitud de la acumulación de neutrófilos.
Entre los días cinco y siete post-infección, se observó un aumento marcado en el número de neutrófilos en el bazo, coincidiendo precisamente con el pico de infiltración pulmonar. Esta sincronía temporal llevó a un análisis transcriptómico comparativo de los subconjuntos de neutrófilos de ambos órganos. Los resultados fueron sorprendentes: los neutrófilos del bazo y del pulmón se dividieron en los mismos tres subconjuntos principales –proliferativo, no activado y activado– y, dentro de cada subconjunto, los perfiles de expresión génica fueron muy similares. Esta similitud transcripcional sugirió fuertemente que los neutrófilos que se acumulan en el bazo durante este período estaban destinados al pulmón.
Para probar directamente si las células del bazo colonizan el pulmón, el equipo empleó datos de transcriptómica espacial del tejido pulmonar, utilizando los conjuntos de datos de una sola célula como referencias para el análisis de deconvolución con el algoritmo Redeconve. Este enfoque permitió la localización precisa de subconjuntos de células de diferentes orígenes dentro de la arquitectura pulmonar. Entre todos los tipos de células inmunitarias examinadas, solo los neutrófilos mostraron una contribución sustancial del bazo. Alrededor de los días cinco a siete post-infección, la proporción de neutrófilos derivados del bazo en el pulmón rivalizó o incluso superó a la de las células derivadas localmente. En contraste, otras poblaciones inmunitarias permanecieron predominantemente derivadas del pulmón, con una mínima contribución del bazo.
La afluencia de neutrófilos del bazo siguió un patrón temporalmente orquestado. En el día cinco, los neutrófilos proliferativos de diferenciación temprana de origen esplénico se enriquecieron en el pulmón. Al día siete, los subconjuntos dominantes cambiaron a neutrófilos esplénicos inmaduros y maduros/ligeramente activados, lo que indica una cadena de suministro continua desde las células progenitoras hasta las células efectoras.
La migración direccional de las células inmunitarias depende de interacciones precisas entre quimiocinas y receptores. El equipo identificó la base molecular de este tráfico de bazo a pulmón. Entre los días cinco y siete post-infección, el tejido pulmonar exhibió una expresión máxima de múltiples quimiocinas atrayentes de neutrófilos, incluyendo Cxcl5, Cxcl12 y Ccl11. Estas quimiocinas fueron producidas por poblaciones de células residentes en el pulmón específicas –células epiteliales, macrófagos y fibroblastos–, cada una contribuyendo con señales distintas.
Simultáneamente, los neutrófilos del bazo en diferentes etapas de diferenciación mostraron una expresión diferencial de los receptores de quimiocinas. Los neutrófilos inmaduros expresaron preferentemente Cxcr4, el receptor de Cxcl12, mientras que los neutrófilos maduros aumentaron la regulación de Cxcr2, Ccr1 y Ccr3, que se unen a Cxcl5, Ccl11 y otras quimiocinas. Esta correspondencia de receptores en las células migrantes con ligandos producidos en el pulmón crea un código de quimiocinas que guía el reclutamiento preciso y específico de la etapa de los neutrófilos del bazo al órgano inflamado.
«Este estudio revisa fundamentalmente la comprensión de la dinámica de los neutrófilos durante las infecciones virales respiratorias«, señaló el profesor Cao. Al integrar la ómica espacial y de una sola célula, el equipo ha demostrado que el bazo funciona como un centro extra-medular para la movilización de neutrófilos, suministrando al pulmón un flujo continuo de células en varias etapas de diferenciación para satisfacer las demandas de la defensa antiviral. Los hallazgos desafían la visión tradicional de que los neutrófilos pulmonares derivan exclusivamente de fuentes locales o de la médula ósea, revelando en cambio una red inter-orgánica coordinada.
«La identificación del eje neutrófilo bazo-pulmón y los pares de quimiocinas-receptores que lo gobiernan abre nuevas vías para la intervención terapéutica«, destacaron los autores. Para las afecciones pulmonares inflamatorias impulsadas por respuestas de neutrófilos excesivas o desreguladas, incluida la neumonía viral grave, la focalización de este eje podría ofrecer un medio para modular el reclutamiento y la actividad de las células inmunitarias. El estudio proporciona un nuevo marco teórico para comprender la coordinación inmunitaria inter-orgánica y destaca posibles objetivos diagnósticos y terapéuticos para las enfermedades infecciosas pulmonares.
Una enzima metabólica estudiada durante más de siete décadas posee una segunda función oculta: puede desenrollar ARN y promover la progresión del ciclo celular, una función adicional a su papel en la producción de energía, según un nuevo estudio liderado por la Universidad de Surrey.
La fosfofructoquinasa (PFK) es la ‘guardiana’ de la glucólisis, la vía metabólica ancestral y evolutivamente conservada que descompone el azúcar para generar energía. En la levadura Saccharomyces cerevisiae, la PFK está compuesta por dos subunidades: Pfk1 (α) y Pfk2 (β). Si bien ambas se han entendido desde hace tiempo como socios metabólicos, el equipo de Surrey ha descubierto que Pfk2 posee una capacidad completamente separada. Se une a cientos de ARN mensajeros (ARNm) dentro de las células, desenrolla ARN de doble cadena corto en una dirección específica y promueve activamente la traducción de genes que impulsan la división celular.
Publicado en Nucleic Acids Research, el estudio muestra que sin Pfk2, las células de levadura crecen más lentamente, se vuelven significativamente más grandes y tienen dificultades para progresar de la fase G1 a la fase S del ciclo celular, un punto de transición crítico donde las células se comprometen con la división. Es crucial destacar que reintroducir una versión de Pfk2 que no puede realizar la glucólisis aún así revirtió estos defectos, confirmando que el papel de la enzima en la división celular es independiente de su función metabólica.
El profesor André Gerber, autor corresponsal del estudio de la Escuela de Ciencias de la Vida de la Universidad de Surrey, dijo:
«La fosfofructoquinasa se ha estudiado intensamente por su papel en el metabolismo desde la década de 1950. Lo que hemos descubierto es que una de sus subunidades, Pfk2, también funciona como un regulador de ARN que ayuda a coordinar cuándo las células se dividen. Esto no se trata de producción de energía; proponemos que la enzima actúa como un relé molecular, detectando el estado energético de la célula y utilizando esa información para decidir si promover el crecimiento.»
El equipo de investigación utilizó una combinación de secuenciación de ARN, ensayos bioquímicos (pruebas de laboratorio para estudiar el comportamiento molecular) y proteómica (análisis a gran escala de proteínas) para construir su caso. Identificaron más de 800 ARNm a los que se une Pfk2 en células vivas, muchos de los cuales codifican proteínas involucradas en el control del ciclo celular mitótico (el proceso por el cual una célula se divide en dos). Utilizando pruebas que utilizan señales de luz para rastrear hebras de ARN que se separan en tiempo real, el equipo de investigación demostró que Pfk2, pero no Pfk1, puede desenrollar moléculas de ARN de doble cadena cortas con una direccionalidad específica, una función normalmente asociada con enzimas helicasas de ARN dedicadas (proteínas especializadas cuyo trabajo principal es desenrollar ARN).
El perfilado de polisomas (una técnica que separa el contenido celular para revelar qué ARNm se están convirtiendo activamente en proteínas) reveló que en las células que carecen de Pfk2, los ARNm de reguladores críticos del ciclo celular, incluido el ciclina G1 CLN3 (una proteína que desencadena el inicio de la división celular) y la proteína de control del huso BUB3 (una proteína que asegura que los cromosomas se separen correctamente), se desplazaron drásticamente lejos de los ribosomas, lo que indica que ya no se estaban traduciendo eficientemente en proteínas. La proteómica confirmó niveles reducidos de proteínas del ciclo celular en mutantes de deleción de Pfk2 (células donde se elimina el gen que codifica Pfk).
El equipo propone un modelo de «interruptor de relé molecular». Cuando la energía celular es baja, la PFK adopta su estado enzimáticamente activo y se centra en la glucólisis. Cuando la energía es abundante, Pfk2 cambia a una forma de baja actividad que mejora su capacidad para unirse y desenrollar ARN, promoviendo la traducción (producción de proteínas a partir de instrucciones de ARN) de genes del ciclo celular y permitiendo la división celular. Esto crea un vínculo molecular directo entre el estado metabólico de una célula y su decisión de proliferar.
Waleed Albihlal, primer autor del estudio e investigador de la Universidad de Surrey, dijo:
«Durante décadas, la PFK se ha descrito en todos los libros de texto de bioquímica como una enzima unifuncional que actúa únicamente en la glucólisis. El descubrimiento de esta función dual de la PFK abre nuevas vías para avanzar en nuestro conocimiento de las funciones celulares críticas. Esto podría, por ejemplo, permitirnos comprender mejor las enfermedades que involucran una desregulación del ciclo celular y conducir al desarrollo de nuevas terapias. Además, este descubrimiento plantea una importante pregunta: ¿cuántas más funciones ocultas existen en otras enzimas que esperan ser descubiertas?»
La investigación fue financiada por el Biotechnology and Biological Sciences Research Council (BBSRC), Cancer Research UK y el Engineering and Physical Sciences Research Council (EPSRC). Los colaboradores internacionales incluyeron equipos del Cancer Research UK Scotland Institute, la Universidad de Osnabrück, la Universidad de Basilea y la Universidad de Ulm.