El ADN tumoral circulante (ctDNA) se ha convertido en una herramienta clave para detectar la enfermedad residual molecular después de una cirugía curativa en casos tempranos de cáncer colorrectal. A menudo, permite identificar la recurrencia meses antes de que se detecte mediante pruebas de imagen tradicionales, lo que influye en las estrategias de quimioterapia adyuvante y de vigilancia. Sin embargo, los médicos deben elegir entre pruebas informadas por el tumor, que son personalizadas y potencialmente más sensibles, y pruebas agnósticas al tumor, que son más rápidas e independientes del tejido, pero podrían no detectar la enfermedad en niveles bajos.
En este metaanálisis de precisión diagnóstica, Camblor y sus colegas demuestran que esta elección depende en gran medida del contexto: durante el monitoreo seriado, las pruebas informadas por el tumor logran una sensibilidad significativamente mayor que los enfoques agnósticos al tumor, sin aumentar los falsos positivos. Esto subraya la importancia de alinear la estrategia de prueba de ctDNA con el objetivo clínico.
Título: Rendimiento clínico de los ensayos de ctDNA informados por el tumor frente a los ensayos agnósticos al tumor para la recurrencia del cáncer colorrectal: una revisión sistemática y un metaanálisis de precisión diagnóstica
Autores: Daniel G. Camblor, Belén Martínez-Castedo, Jorge Martín-Arana, Francisco Gimeno-Valiente, Blanca García-Micó, Francisco Martínez-Picó, Víctor Segu, Miguel García-Bartolomé, Diego González, Alejandro Guimera, Marisol Huerta, Susana Roselló, Valentina Gambardella, Desamparados Roda, Leontios Pappas, Aparna Parikh, Juan Antonio Carbonell-Asins, Andrés Cervantes, Noelia Tarazona.
Antecedentes
Después de una cirugía con intención curativa para el cáncer colorrectal en estadio I-III, el principal problema clínico es identificar a los pacientes que aún presentan enfermedad residual molecular (ERM) y, por lo tanto, tienen un alto riesgo de recurrencia, a menudo meses antes de que las pruebas de imagen sean positivas. El ADN tumoral circulante (ctDNA) ha surgido como una herramienta práctica para la ERM, con el fin de refinar las decisiones sobre la quimioterapia adyuvante y mejorar la vigilancia. Sin embargo, los médicos se enfrentan a una elección real entre los ensayos informados por el tumor (IT), personalizados según las mutaciones del tumor del paciente, y los ensayos agnósticos al tumor (TA), que utilizan solo plasma o paneles fijos (a menudo incluyendo estrategias de metilación/fragmentómica) y son más fáciles de implementar cuando el tejido es limitado.
Esta revisión sistemática y metaanálisis de precisión diagnóstica comparó directamente el rendimiento de IT y TA para detectar la recurrencia y, lo que es más importante, probó cómo la estrategia de muestreo (una prueba “de referencia” postoperatoria única frente a pruebas “seriadas” repetidas) cambia la sensibilidad y las tasas de falsos positivos en la práctica.
Métodos
Los autores realizaron una búsqueda sistemática en PubMed y Embase hasta el 31 de octubre de 2025, restringida a textos completos en inglés a partir de 2015, centrándose en el cáncer colorrectal resecado en el entorno postoperatorio y requiriendo datos de precisión diagnóstica 2×2 extraíbles (verdaderos/falsos positivos/negativos) para la detección de recurrencia. La presentación de los estudios siguió PRISMA-DTA y el riesgo de sesgo se evaluó utilizando QUADAS-2. Para la síntesis cuantitativa, utilizaron (1) un enfoque univariado de efectos aleatorios para explorar las relaciones de probabilidad diagnóstica (DOR) y el sesgo de publicación (prueba de Deeks), y (2) el modelo bivariado de efectos aleatorios de Reitsma para estimar conjuntamente la sensibilidad y la tasa de falsos positivos (FPR = 1-especificidad) y para comparar IT y TA dentro de los entornos de referencia y seriado.
Diseño del Estudio
Este fue un metaanálisis de revisión sistemática con precisión diagnóstica (no un ensayo terapéutico). En todos los estudios elegibles, los autores incluyeron 33 estudios que evaluaron el ctDNA para la detección de recurrencia después de una cirugía con intención curativa para el cáncer colorrectal. La implementación en el mundo real se abordó explícitamente estratificando los estudios en: pruebas de referencia (un punto temporal postoperatorio único, generalmente semanas después de la cirugía) frente a pruebas seriadas (muestreo longitudinal durante el seguimiento). La comparación principal fue IT frente a TA, y la principal pregunta de diseño fue si el tipo de ensayo importa más o menos que la estrategia de muestreo.
Resultados
Volumen del estudio y escenarios clínicos representados. De 623 registros, se incluyeron 33 estudios. Para los análisis de referencia, 27 estudios aportaron datos de 7.482 pacientes con 1.488 eventos de recurrencia. Para los análisis seriados, 17 estudios incluyeron 2.865 pacientes con 561 recurrencias, lo que refleja menos conjuntos de datos, pero una mayor alineación con la forma en que el ctDNA se utiliza a menudo para la vigilancia continua.
La estrategia de muestreo cambió la sensibilidad más que los falsos positivos. En el marco bivariado, las pruebas seriadas mejoraron la sensibilidad en comparación con las pruebas de referencia única (0,72 frente a 0,51, p = 0,001), mientras que las diferencias en las tasas de falsos positivos no fueron estadísticamente significativas entre las estrategias. Esto apoya un punto clínicamente intuitivo: el muestreo repetido aumenta la probabilidad de detectar el ctDNA a medida que la eliminación del tumor evoluciona con el tiempo, sin aumentar claramente la carga de falsas alarmas.
Informado por el tumor frente a agnóstico al tumor: dónde la diferencia se vuelve decisiva. Cuando el análisis se estratificó por entorno, la principal separación apareció en el escenario seriado. En el monitoreo seriado, los ensayos IT mostraron una sensibilidad marcadamente mayor que los ensayos TA (0,88 frente a 0,59, p = 0,001). Es importante destacar que esta ganancia no vino acompañada de una tasa de falsos positivos estadísticamente mayor: la FPR fue de 0,09 para IT frente a 0,12 para TA (p = 0,419). En otras palabras, las pruebas IT seriadas fueron sustancialmente mejores para identificar las verdaderas recurrencias manteniendo un perfil de falsos positivos similar.
En las pruebas de referencia (un único punto temporal), IT no superó a TA. En los estudios de referencia única, las estimaciones de sensibilidad fueron de 0,48 para IT frente a 0,58 para TA (p = 0,070) y las FPR fueron similares (0,08 frente a 0,10, p = 0,329). Prácticamente, esto sugiere que cuando solo es factible un resultado de ctDNA postoperatorio único (a menudo el escenario vinculado a decisiones adyuvantes sensibles al tiempo), la selección del ensayo puede depender más de la logística (disponibilidad de tejido, tiempo de respuesta) que de la expectativa de una precisión diagnóstica claramente superior de un enfoque.
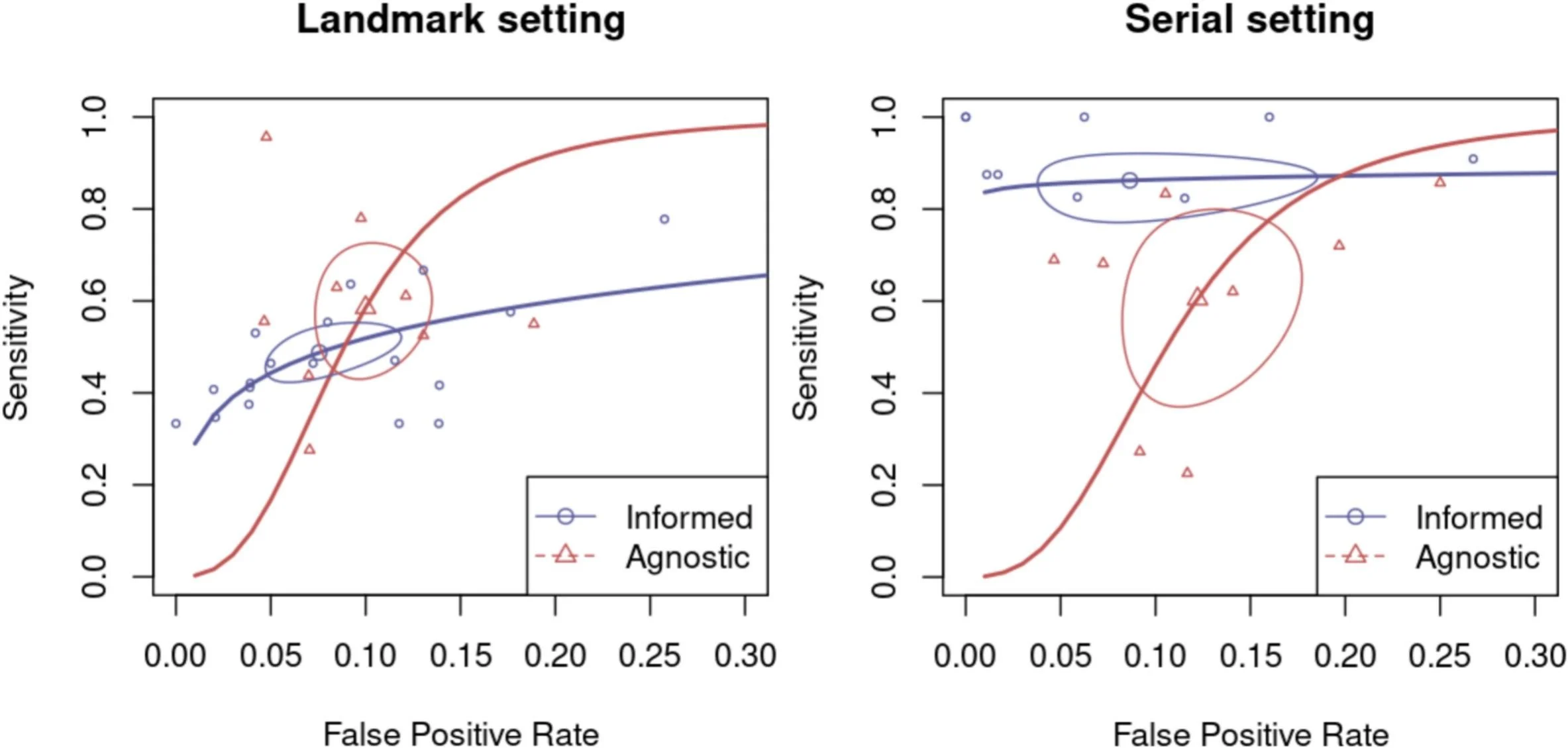
Señales exploratorias de DOR y sesgo de publicación. En los análisis univariados, los estudios de referencia mostraron relaciones de probabilidad diagnóstica (DOR) agrupadas similares para IT y TA, mientras que los estudios seriados favorecieron a IT con una señal de DOR agrupada mucho mayor. Sin embargo, la prueba de Deeks sugirió un sesgo de publicación en el conjunto de datos seriado (los estudios más pequeños tendían a “superar el rendimiento”), lo que los autores señalan adecuadamente como una precaución al interpretar la magnitud de la ventaja, sin negar la dirección constante de una mejor sensibilidad para IT en el monitoreo seriado.
Hallazgos Clave
- El muestreo seriado mejora significativamente la sensibilidad de la detección de recurrencia en comparación con una prueba de referencia única, lo que refuerza que la frecuencia con la que se realiza la prueba afecta materialmente el rendimiento del ctDNA.
- En la vigilancia seriada, el ctDNA informado por el tumor es sustancialmente más sensible que los enfoques agnósticos al tumor (0,88 frente a 0,59) manteniendo tasas de falsos positivos similares, lo que apoya a IT como la opción más confiable cuando el monitoreo longitudinal es factible.
- En la ventana postoperatoria de referencia, no se demostró una ventaja diagnóstica estadísticamente significativa para IT sobre TA, lo que mantiene a los enfoques TA relevantes clínicamente cuando no hay tejido tumoral disponible o las decisiones deben tomarse rápidamente.
Conclusión
Este metaanálisis de precisión diagnóstica proporciona un marco clínicamente práctico para seleccionar los ensayos de ctDNA después de la resección de CRC: la estrategia de muestreo influye fuertemente en el rendimiento, y las pruebas informadas por el tumor fortalecen claramente la sensibilidad en el monitoreo seriado (0,88 frente a 0,59) sin empeorar significativamente las tasas de falsos positivos. Por el contrario, cuando el ctDNA se utiliza como una prueba postoperatoria de referencia única, IT no demuestra una ventaja estadísticamente significativa sobre TA, lo que hace que las limitaciones del mundo real (particularmente la disponibilidad de tejido tumoral y el tiempo) sean centrales para la toma de decisiones.
Puede leer el artículo completo aquí.

