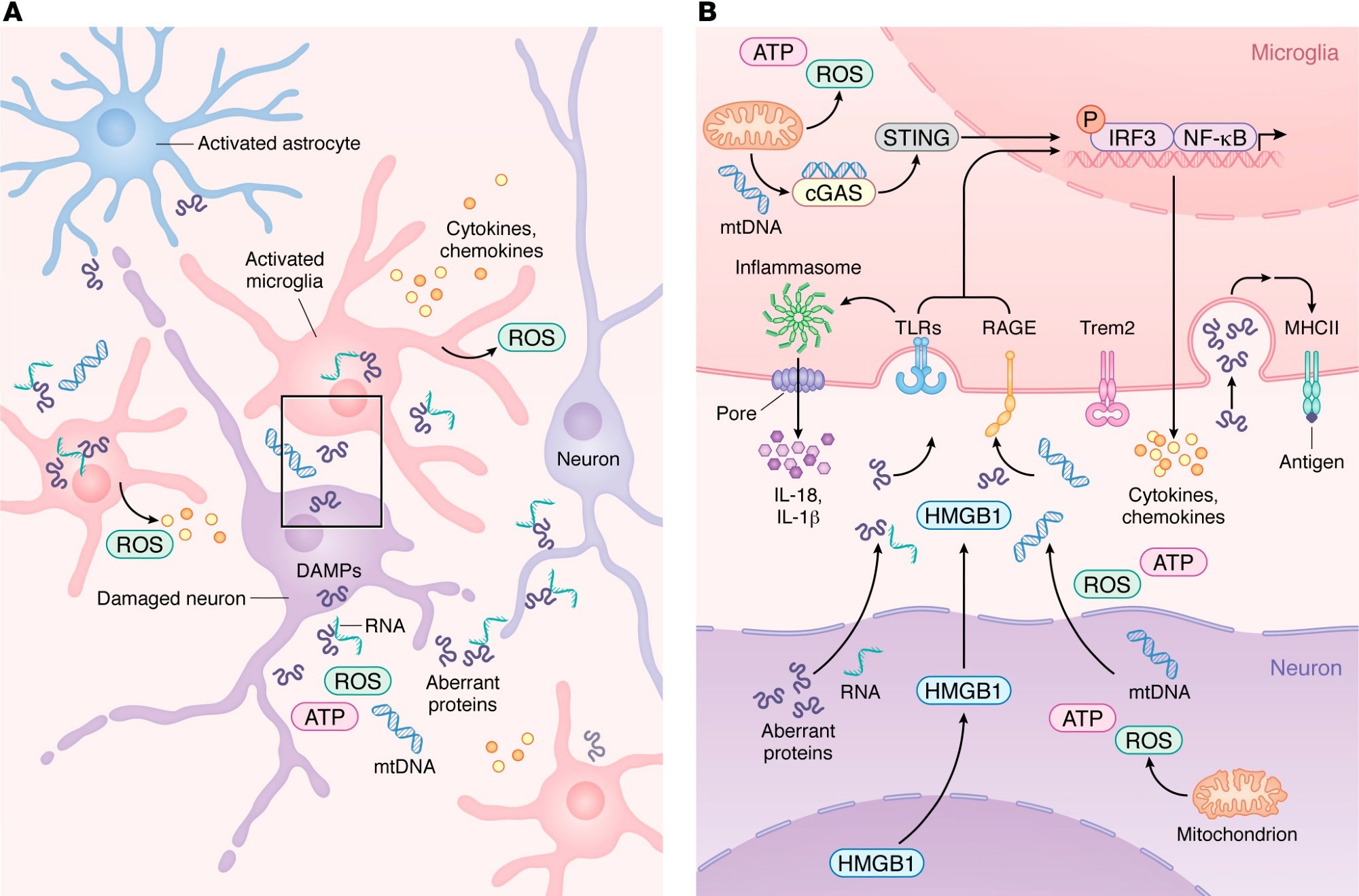
Un amplio estudio publicado recientemente revela cómo el sistema inmunológico del cerebro puede tanto combatir como contribuir al desarrollo de enfermedades neurodegenerativas como el Alzheimer, el Parkinson y trastornos relacionados. La investigación destaca que el momento, el tipo de célula involucrada y el contexto específico de la enfermedad son factores cruciales que podrían determinar el éxito de futuras terapias inmunomoduladoras.
La terapia génica ha demostrado ser exitosa en el tratamiento de diversas enfermedades, incluyendo inmunodeficiencias, ceguera hereditaria, hemofilia y, más recientemente, la enfermedad de Huntington, un trastorno neurológico fatal.
Un avance publicado en la revista Neuron refuerza la evidencia de que esta técnica podría desbloquear terapias personalizadas potentes. Bioingenieros de la Universidad de Rice, liderados por Jerzy Szablowski, en colaboración con investigadores del laboratorio de Vincent Costa en la Universidad de Emory, han descubierto que los marcadores de actividad liberados (RMAs) – proteínas diseñadas para cruzar la barrera hematoencefálica y permanecer en la sangre durante horas, proporcionando una forma fiable y no invasiva de obtener información sobre la expresión génica en el cerebro – funcionan tan bien en monos como en ratones.
Los estudios en modelos animales grandes son una parte crítica del proceso para llevar un descubrimiento de laboratorio a un tratamiento que salve vidas. La mayoría de las investigaciones no llegan a esta etapa.
«Nuestro estudio demuestra que es relativamente fácil trasladar esta técnica no invasiva entre especies», afirmó Szablowski. «Esto es emocionante porque los RMAs son una herramienta extremadamente sensible que podría utilizarse para rastrear tan solo decenas o cientos de neuronas a la vez, algo que ninguna técnica de imagen o monitoreo existente puede lograr con ese nivel de precisión.»
Además de la precisión, la tecnología RMA también es versátil y adaptable: se pueden diseñar diferentes marcadores séricos para rastrear múltiples genes en diferentes regiones del cerebro.
«La detección de proteínas puede ser multiplexada», explicó Szablowski. «En el futuro, debería ser posible detectar un gran número de diferentes marcadores séricos sintéticos en una sola muestra utilizando una variedad de técnicas bioquímicas, como la espectrometría de masas o la secuenciación de proteínas de una sola molécula.»
Monitorear la expresión génica en el cerebro vivo e intacto podría revelar información crucial sobre la actividad celular, los procesos cognitivos complejos y cómo se inician y progresan las enfermedades neurológicas. Al obtener esta información mediante un simple análisis de sangre, se vuelve factible rastrear el mismo cerebro individual a lo largo del tiempo.
«En la investigación cerebral, el monitoreo longitudinal es especialmente importante», señaló Szablowski, citando la adicción como ejemplo. «Las lecturas terminales o las biopsias son instantáneas. Al monitorear al mismo individuo a lo largo del tiempo, podemos ver los efectos posteriores de la expresión génica y cómo moldean la enfermedad o la fisiología futura.»
«Para comprender afecciones como la adicción, se necesita más que una sola instantánea del cerebro. Necesitamos ver la película, no solo una fotografía. El seguimiento del cerebro vivo a lo largo del tiempo nos permite observar realmente qué genes impulsan estos cambios a medida que ocurren.»
Szablowski desarrolló la plataforma RMA basándose en la observación de que las terapias con anticuerpos fracasaban porque los anticuerpos se migraban rápidamente del cerebro al torrente sanguíneo. Se centró en la parte de los anticuerpos que les permite cruzar la barrera hematoencefálica y la utilizó como base para los reporteros sintéticos.
«Es una pequeña parte de una proteína que es responsable de la salida de la proteína de la célula al espacio entre células, a la matriz extracelular», explicó Szablowski. «Simplemente cambiar la versión del ratón de este dominio de proteína por la versión del macaco rhesus fue suficiente para que el reportero fuera funcional en la otra especie.»
Costa, coautor principal y colaborador en el estudio, es profesor asociado de psiquiatría y ciencias del comportamiento en Emory. Él y Szablowski comenzaron a colaborar después de que Costa leyera un preimpreso del artículo en el que Szablowski describió por primera vez la plataforma RMA y decidió que quería probarla en un modelo animal grande. Los dos comenzaron a trabajar juntos de inmediato, lo que resultó en el artículo actual, un testimonio de cómo la ciencia abierta puede ayudar a acelerar el progreso de la investigación.
«Al eliminar el cuello de botella de la imagen cerebral compleja y repetida, esta plataforma cambia por completo las matemáticas para la neurociencia de primates», dijo Costa. «Ahorra tiempo y recursos cruciales, lo que nos permite llevar a cabo los estudios a largo plazo y complejos necesarios para cerrar la brecha entre los modelos animales y los tratamientos humanos.»
La investigación fue apoyada por la Fundación David y Lucile Packard (2021-73005) y los Institutos Nacionales de la Salud (R01MH125824, P51OD011132, P51OD011092). El contenido de este comunicado de prensa es responsabilidad exclusiva de los autores y no representa necesariamente las opiniones oficiales de las entidades financiadoras.
Un estudio reciente publicado en la revista Nature ha delineado la neurogénesis en el hipocampo humano a lo largo de la edad adulta, el envejecimiento y la enfermedad de Alzheimer (EA), al tiempo que señala que la relevancia funcional de estos procesos para la cognición humana aún no se comprende completamente.
Antecedentes: Neurogénesis en roedores versus humanos
Los mecanismos epigenéticos y transcripcionales subyacentes a la generación de neuronas a partir de células madre neurales (CMN) están bien establecidos en roedores. La neurogénesis hipocampal desempeña un papel vital en la memoria y el aprendizaje al reclutar neuronas inmaduras en circuitos de memoria y promover la formación de la memoria. La neurogénesis disminuye con la edad y se ve afectada en modelos de EA en ratones.
En contraste, el destino de la neurogénesis en humanos está poco definido. La ocurrencia de neurogénesis en el hipocampo adulto ha sido objeto de debate. Se ha confirmado la presencia de neuronas inmaduras en el cerebro humano adulto y en la EA. Un subconjunto de células progenitoras muestra signos de proliferación continua en el cerebro humano adulto; sin embargo, persisten lagunas clave en el conocimiento, particularmente con respecto a cómo estas firmas moleculares se traducen en resultados cognitivos funcionales.
Perfilado multi-ómico de un solo núcleo del hipocampo humano
Los investigadores analizaron núcleos aislados de hipocampos post mortem humanos utilizando un ensayo de accesibilidad de la cromatina con secuenciación de transposasa (snATAC-seq) y secuenciación de ARN de un solo núcleo (snRNA-seq). Se analizaron perfiles de secuencia de 85.977 núcleos de adultos jóvenes con memoria intacta, denominados la cohorte de adultos jóvenes, para establecer vías reguladoras neurogénicas.
La agrupación no supervisada de datos de snRNA-seq identificó 12 tipos de células en el hipocampo, incluidos neuroblastos, astrocitos, neuronas inmaduras, células granulares maduras, células progenitoras de oligodendrocitos y oligodendrocitos maduros. Los análisis de expresión diferencial de genes y de vías identificaron 169 vías y 4.166 genes expresados diferencialmente (DEG), todos ellos sobreexpresados en neuroblastos en comparación con los oligodendrocitos maduros.
Trayectorias de desarrollo y análisis de velocidad de ARN
Se examinaron los tiempos latentes de los grupos de neuroblastos, astrocitos, células granulares maduras y neuronas inmaduras para identificar las CMN y sus trayectorias de desarrollo utilizando el análisis de velocidad de ARN. Esto mostró un flujo direccional desde las CMN hacia los astrocitos y hacia los neuroblastos hasta las células granulares maduras a través de las neuronas inmaduras. Las CMN expresaron bajos niveles de marcadores neuronales, pero altos niveles de sustitutos de la pluripotencia en comparación con las neuronas inmaduras y los neuroblastos.
El análisis snATAC-seq permitió una evaluación ortogonal de la pluripotencia a través de la accesibilidad de la cromatina. Se observó una alta accesibilidad de la cromatina en regiones asociadas con el potencial multilineal en las CMN. En contraste, los sustitutos de la maduración neuronal mostraron altos niveles de cromatina abierta en las neuronas inmaduras y los neuroblastos. Las regiones de accesibilidad diferencial (DAR) y los DEG superiores en las CMN se redujeron en las neuronas inmaduras y los neuroblastos.
Por el contrario, las DAR y los DEG superiores en los neuroblastos se redujeron en las CMN. Los DEG superiores en las neuronas inmaduras tenían baja expresión en las CMN y expresión moderada en los neuroblastos. Las vías de desarrollo se redujeron en las neuronas inmaduras y los neuroblastos, pero se enriquecieron en las CMN. Los motivos superiores en las CMN incluyeron el transductor de señal y el activador de la transcripción 3 (STAT3), STAT4, STAT5, factor nuclear I B (NFIB) y gen similar a adenoma pleomórfico 1 (PLAGL1).
En las neuronas inmaduras, los motivos superiores incluyeron el factor nuclear eritroide 2 (NFE2), PBX homeobox 2 (PBX2), Meis homeobox 2 (MEIS2) y factor regulador X2 (RFX2). Estos patrones sugieren un cambio de factores de transcripción que promueven la proliferación y el mantenimiento de las CMN a aquellos que regulan la diferenciación y la maduración en las neuronas inmaduras. Los investigadores examinaron entonces los efectos del diagnóstico cognitivo y la edad en la neurogénesis.
Neurogénesis a través del envejecimiento, la patología preclínica y la enfermedad de Alzheimer
Se secuenciaron núcleos hipocampales de personas mayores sanas sin deterioro cognitivo, adultos con EA y adultos con patología intermedia preclínica. También se analizaron muestras de SuperAgers. Estos individuos tenían 80 años o más y obtuvieron resultados en pruebas de memoria episódica comparables o mejores que los de personas de entre 50 y 59 años. Todos los tipos de células detectados en la cohorte de adultos jóvenes se observaron en estos grupos.
Los grupos de EA y patología preclínica tenían significativamente más CMN que las personas mayores sanas. La cohorte de EA tenía significativamente menos neuronas inmaduras y neuroblastos que los adultos jóvenes y las personas mayores sanas, y menos neuronas inmaduras que el grupo de patología preclínica. La mayoría de los cambios relacionados con el diagnóstico y la edad se observaron en los recuentos de DAR en lugar de los recuentos de DEG, lo que destaca la accesibilidad de la cromatina como un discriminador más fuerte de las trayectorias cognitivas que la abundancia de transcritos.
Un subconjunto de DAR se redujo específicamente en las neuronas inmaduras y los neuroblastos en el grupo de patología preclínica en comparación con los SuperAgers, las personas mayores sanas y los adultos jóvenes. Estas DAR se redujeron aún más en la EA. Estos hallazgos sugieren que las alteraciones en la accesibilidad de la cromatina pueden contribuir a trayectorias neurogénicas interrumpidas durante el deterioro cognitivo. Algunos de los primeros cambios relacionados con la edad fueron detectables en la accesibilidad de la cromatina en la etapa de las CMN.
Firmas de resiliencia cognitiva en los SuperAgers
La cohorte de SuperAgers exhibió un número significativamente mayor de neuronas inmaduras en comparación con otros grupos y más neuroblastos que la cohorte de EA. Este perfil fue atribuible a los patrones de DAR. La cohorte de SuperAgers tenía 7.058 y 674 DAR sobreexpresados en neuronas inmaduras y neuroblastos, respectivamente, en comparación con otras cohortes.
Se calcularon puntuaciones de resiliencia para detectar la direccionalidad consistente de los efectos de la cromatina y la transcripción en las cohortes en lugar de medir directamente el rendimiento cognitivo. Se observó una firma clara en las neuronas inmaduras y los neuroblastos, con la mayoría de los picos y genes permaneciendo estables en los SuperAgers, los adultos jóvenes y las personas mayores sanas, pero reducidos en la EA.
Análisis adicionales indicaron que la preservación de la integridad de las sinapsis excitatorias era una característica del envejecimiento cognitivo saludable. Las interacciones regulatorias que involucran a los astrocitos y las neuronas piramidales de CA1 también distinguieron el envejecimiento exitoso del envejecimiento patológico. Los autores señalan que los tamaños de cohorte relativamente pequeños y la considerable variabilidad interindividual justifican una interpretación cautelosa.
Conclusiones e implicaciones terapéuticas
El estudio delineó firmas moleculares de la neurogénesis en el hipocampo humano y sus cambios a lo largo de la edad y el estado cognitivo. Las diferencias en la accesibilidad de la cromatina a lo largo del espectro neurogénico sugieren que las alteraciones epigenéticas pueden ser firmas más definitivas de las trayectorias cognitivas asociadas al envejecimiento que los cambios en la expresión génica. La delimitación de estos mecanismos y su interacción con la dinámica de la red hipocampal más amplia puede informar estrategias terapéuticas dirigidas a preservar la función cognitiva en el envejecimiento. Sin embargo, se necesita más investigación para establecer vínculos causales entre estos patrones moleculares y el rendimiento cognitivo.